Considere as afirmações abaixo sobre as Lagoas de Maturação utilizadas no tratamento de esgotos:
I. Seu principal objetivo é a remoção de patogênicos.
II. Possui condições adversas aos microrganismos, como elevada radiação e pH.
III. É empregada principalmente como pós-tratamento aos processos que reduzem a Demanda Bioquímica de Oxigênio (DBO).
Está correto o que se afirma em
Nesse tipo de tratamento a matéria orgânica é estabilizada pela ação de organismos aeróbios que se encontram aderidos a um meio suporte que pode ser de pedras ou plástico.
O texto refere-se a
Considere a ilustração abaixo.
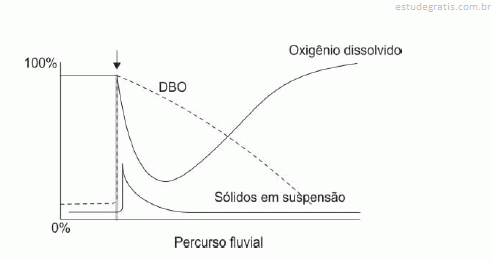
O evento indicado pela seta representa:
Numa estação de tratamento de esgotos, o biogás gerado como produto da degradação microbiológica do lodo é produzido em ...... e é composto principalmente por ...... que pode ser utilizado como combustível.
As lacunas são, correta e respectivamente, preenchidas por:
As estações de tratamento de esgoto, na sua maioria, fazem o tratamento e o posterior despejo em um corpo receptor (rio, riacho, lagoa, etc.) e têm uma especial atenção com os resíduos gerados no processo de tratamento, principalmente o lodo.
Apesar de ser constituído em sua maior parte por matéria orgânica, o lodo representa riscos ao meio ambiente e, se mal destinado, pode contaminar solos ou outras áreas se for arrastado por água de chuva. Considere as afirmativas abaixo.
I. O lodo pode ser despejado no corpo receptor (rio, riacho, lago, etc.) para degradação da matéria orgânica pelos microrganismos presentes na água.
II. O lodo pode ser enviado para tratamento térmico (incineração).
III. O lodo pode ser enviado para agricultores próximos à estação...