501
Q952368
Considere um elemento químico, genericamente nomeado X. Sua massa é igual a 56 e o número de nêutrons igual a 30. O número de elétrons desse elemento químico em estado X2+ será:
502
Q952367
Considere os seguintes óxidos:
I. SO3 II. Al2O3 III. NO2 IV. Fe3O4 V. Na2O2 VI. Na2O
Sobre as propriedades dessas substâncias químicas, assinale a alternativa correta.
I. SO3 II. Al2O3 III. NO2 IV. Fe3O4 V. Na2O2 VI. Na2O
Sobre as propriedades dessas substâncias químicas, assinale a alternativa correta.
503
Q952366
Considere a seguinte reação química, não-balanceada.
C2H6O + O2 ? CO2 + H2O
Para a reação descrita, 3,0 g de C2H6O foi adicionado a um ambiente contendo 100,0 g de oxigênio. A massa (g) de CO2 produzida será, aproximadamente, de:
Dados de massas molares: C = 12 g/mol, H = 1 g/mol e O = 16 g/mol.
C2H6O + O2 ? CO2 + H2O
Para a reação descrita, 3,0 g de C2H6O foi adicionado a um ambiente contendo 100,0 g de oxigênio. A massa (g) de CO2 produzida será, aproximadamente, de:
Dados de massas molares: C = 12 g/mol, H = 1 g/mol e O = 16 g/mol.
504
Q952365
Considere a estrutura química da testosterona.
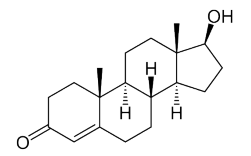
A massa molar para a estrutura química fornecida na imagem será, aproximadamente, de:
Dados de massas molares: C = 12 g/mol, H = 1 g/mol e O = 16 g/mol.
505
Q952364
Alotropia é o fenômeno que ocorre quando um elemento químico forma duas ou mais substâncias simples diferentes. Acerca do tema, assinale a alternativa que apresenta uma substância considerada forma alotrópica do grafite.
506
Q952363
Sabendo que o elemento químico Prata apresenta número atômico 47, a representação do nível eletrônico ocupado mais externo (nível de valência) para este átomo (neutro) está corretamente apresentado em:
507
Q952312
Um tanque de armazenamento contém inicialmente 300 mol de C2H6 (g) a 1,3 atm. 150 mol adicionais de C2H6 (g) são bombeados para o tanque à temperatura constante, que é grande suficiente para manter a temperatura também constante. Sabendo-se que a massa molar do C2H6 (g) é de 30,07 g/mol e a constante universal dos gases é 0,082 atm.l.mol-1.K-1 , assinale a alternativa que corresponde à pressão final dentro do tanque:
508
Q952311
Em um experimento à temperatura constante, duas situações foram testadas ao mesmo tempo. Um gás A, que estava em um container de 750 ml e uma pressão de 1000 Torr foi transferido para um recipiente de 5 l. Um gás B com um volume inicial de 0,7 l a 600 Pa foi comprimido a 200 ml. Sabe-se que a massa molar do gás A é 76 g/mol e do gás B é 132 g/mol e as constantes universais dos gases é 62,3637 L.Torr.K-1 .mol-1 e 8,314462 m3.Pa.K-1.mol-1.
Considerando essa situação, assinale a alternativa que contenha as pressões finais dos dois gases corretas.
Considerando essa situação, assinale a alternativa que contenha as pressões finais dos dois gases corretas.
509
Q952310
Um experimento com um gás inerte foi conduzido, a partir de 500 ml desse gás a uma temperatura de 300K foi observada uma pressão de 100 KPa. Para observar suas propriedades, esse mesmo gás foi comprimido a 250 ml e levado à temperatura de 270K. Com esses dados expostos, analise as afirmativas a seguir. A constante universal dos gases é 8,314462 L.kPa.K-1.mol-1 .
I. A pressão final será menor que a inicial pois houve a diminuição da temperatura do experimento. II. A pressão final será maior apesar de haver a diminuição da temperatura do experimento. III. A pressão final será menor que a inicial, pois na reação que ocorre no experimento, o número de mols do gás diminui, conforme Lei de Avogadro. IV. Não há alteração na pressão final, pois com a reação que ocorre no experimento, o núme...
I. A pressão final será menor que a inicial pois houve a diminuição da temperatura do experimento. II. A pressão final será maior apesar de haver a diminuição da temperatura do experimento. III. A pressão final será menor que a inicial, pois na reação que ocorre no experimento, o número de mols do gás diminui, conforme Lei de Avogadro. IV. Não há alteração na pressão final, pois com a reação que ocorre no experimento, o núme...
510
Q952309
Observe as seguintes situações:
1. 40,0 mg de Ar está confinado em um frasco de 0,0500 l a 27°C. 2. 40,0 mg de Kr está confinado em um frasco diferente de 0,0500 l a 27ºC.
A constante universal dos gases é 8,314462 L.kPa.K-1.mol-1. Massa molar aproximada: Ar = 40 g/mol, Kr = 80 g/mol.
Sobre o assunto, analise as afirmativas a seguir.
I. Para ter a mesma pressão do Ar, o Kr tem que estar a 600K. II. Para que os 2 gases tenham a mesma pressão, as temperaturas do Ar e do Kr devem ser iguais. III. O número de mol (n) do Kr é o dobro do número de mols do At.
Estão corretas as afirmativas:
1. 40,0 mg de Ar está confinado em um frasco de 0,0500 l a 27°C. 2. 40,0 mg de Kr está confinado em um frasco diferente de 0,0500 l a 27ºC.
A constante universal dos gases é 8,314462 L.kPa.K-1.mol-1. Massa molar aproximada: Ar = 40 g/mol, Kr = 80 g/mol.
Sobre o assunto, analise as afirmativas a seguir.
I. Para ter a mesma pressão do Ar, o Kr tem que estar a 600K. II. Para que os 2 gases tenham a mesma pressão, as temperaturas do Ar e do Kr devem ser iguais. III. O número de mol (n) do Kr é o dobro do número de mols do At.
Estão corretas as afirmativas: