31
Q1058227
O reativo de Kastle-Meyer é frequentemente utilizado para a detecção de sangue em amostras. Nesse teste, uma gota do reativo é colocado em uma amostra coletada via swab umedecido e na sequência adiciona-se uma gota de água oxigenada. O reativo é uma solução incolor com fenolftaleína, quando há indício de sangue a cor rósea aparece na amostra. A figura abaixo mostra a reação da fenolftaleína (A), que ao liberar um H+ se transforma em um ânion (B) responsável pela mudança de coloração do meio.
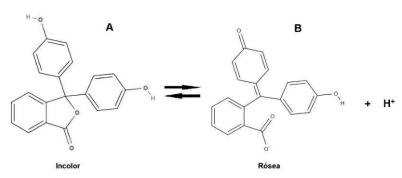
Sobre as espécies envolvidas na reação acima, assinale a alternativa correta:

Sobre as espécies envolvidas na reação acima, assinale a alternativa correta: