391
Q676657
Considere que a concentração de equilíbrio dos íons Cr3+ em uma solução saturada de Cr(IO3)3 (iodato de cromo), a uma dada temperatura T, seja de 0,0200 mol/L. Com relação ao iodato de cromo e à solução em questão, julgue os itens a seguir. A constante do produto de solubilidade (Kps) do Cr(IO3)3, na temperatura T, é maior que 1,0 × 10-6.
392
Q676656

O processo de corrosão de um metal M qualquer pela chuva ácida pode ser corretamente representado pela seguinte equação química.
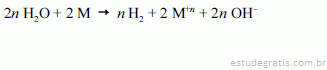
393
Q676655
 No processo de corrosão de uma superfície metálica, o metal é o agente oxidante.
No processo de corrosão de uma superfície metálica, o metal é o agente oxidante.
394
Q676654
 Quanto maior for a energia de ionização do metal constituinte da superfície metálica, menor será o potencial de sua reação de corrosão pela chuva ácida.
Quanto maior for a energia de ionização do metal constituinte da superfície metálica, menor será o potencial de sua reação de corrosão pela chuva ácida.
395
Q676653
Considerando os compostos NH3, H2O, HF, H2S e SF4 e os elementos químicos envolvidos em suas composições, julgue os itens seguintes. A ordem crescente dos comprimentos das ligações entre o H e os átomos de O, N e F nos compostos em questão é: F—H < O—H < N—H.
396
Q676652
Considerando os compostos NH3, H2O, HF, H2S e SF4 e os elementos químicos envolvidos em suas composições, julgue os itens seguintes. A ligação S—H apresenta maior energia de dissociação que a ligação O—H.
397
Q676651
Considerando os compostos NH3, H2O, HF, H2S e SF4 e os elementos químicos envolvidos em suas composições, julgue os itens seguintes. A similaridade das fórmulas moleculares dos compostos H2S e H2O está relacionada ao fato de que átomos de enxofre e oxigênio possuem o mesmo número de elétrons de valência.
398
Q676650
Considerando os compostos NH3, H2O, HF, H2S e SF4 e os elementos químicos envolvidos em suas composições, julgue os itens seguintes. 

399
Q676649
Considerando os compostos NH3, H2O, HF, H2S e SF4 e os elementos químicos envolvidos em suas composições, julgue os itens seguintes. De acordo com a teoria da repulsão entre os pares de elétrons da camada de valência, a molécula de SF4 apresenta geometria tetraédrica.
400
Q676648
Considere que 20,00 mL de uma solução aquosa de NH3 foram titulados com uma solução aquosa de HCl 0,100 mol/L, usandose fenoftaleína como indicador ácido-base, cuja mudança de coloração ocorre no intervalo de pH entre 8,2 e 10. Acerca dessa titulação, julgue os itens a seguir. Se 16,70 mL da solução de HCl foram gastos até se atingir o ponto de equivalência da titulação, então a concentração da solução de NH3 é maior que 0,0800 mol/L.