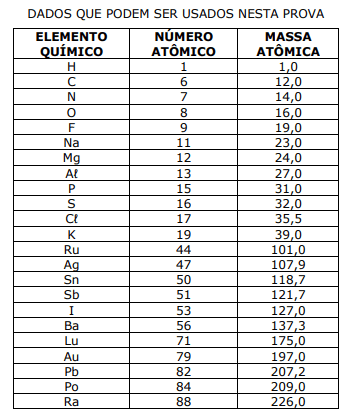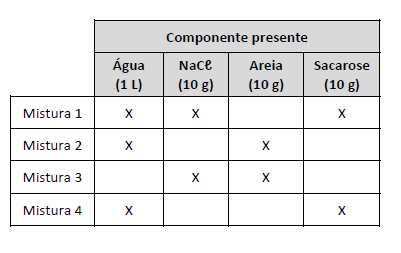
O quadro acima apresenta quatro diferentes misturas realizadas, indicando com um “X” os componentes presentes em cada mistura. Em todas as misturas, os componentes foram colocados em contato e agitados por um tempo, observando‐se, em seguida, os resultados.
Acerca dos resultados observados após a realização das misturas indicadas no quadro, julgue os seguintes itens.
Apenas as misturas 1 e 4 são homogêneas, pois os componentes sólidos que foram misturados apresentam solubilidade em água, formando uma solução aquosa.