21
Q826892
Quanto a compostos orgânicos e a reações de caracterização, julgue os itens de 113 a 116. A identificação de compostos insaturados é possível por meio das reações de adição. No método com adição de bromo em tetracloreto de carbono, o teste será positivo se a solução se descolorar imediatamente, com formação de precipitado marrom. No teste com permanganato, será positivo se ocorrer a descoloração da solução, que é avermelhada. Ambos os testes confirmam a presença de insaturação.
22
Q826891
Acerca de eletroquímica e de processos de oxidação e redução, julgue os itens de 107 a 112. Célula eletroquímica é um dispositivo ou sistema que converte energia elétrica em química ou vice‐versa, formado por dois eletrodos em contato com um eletrólito. Em uma pilha galvânica, um conjunto de células eletroquímicas é usado para a produção de eletricidade como resultado de uma reação química espontânea. Em uma célula eletrolítica, a corrente elétrica é usada para produzir uma transformação química.
23
Q826890
Acerca de eletroquímica e de processos de oxidação e redução, julgue os itens de 107 a 112. As espécies capazes de fixar elétrons são agentes redutores e as capazes de doar elétrons são agentes oxidantes. Um agente redutor age recebendo elétrons de uma espécie. Com isso, ele reduz essa espécie e ele próprio é oxidado.
24
Q826889
Acerca de eletroquímica e de processos de oxidação e redução, julgue os itens de 107 a 112. As reações de oxidação e redução envolvem a transferência de elétrons de uma espécie molecular ou iônica para outra. A redução é a perda de elétrons por uma dada espécie e a oxidação é a fixação desses elétrons por uma determinada espécie.
25
Q826888
Acerca de eletroquímica e de processos de oxidação e redução, julgue os itens de 107 a 112. Eletroquímica é a parte da química que trata do uso das reações químicas para produzir eletricidade, das capacidades relativas de oxidação e redução e do uso da eletricidade para produzir uma transformação química.
26
Q826887
Julgue os itens de 101 a 106, relativos a ácidos e bases. A solução‐tampão é aquela cujo pH é mantido constante quando pequenas quantidades de ácido ou base são adicionadas. Um tampão básico, que estabiliza soluções em pH > 7, é preparado com uma solução que contém 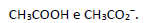
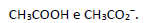
27
Q826886
Julgue os itens de 101 a 106, relativos a ácidos e bases. Indicadores ácido‐base são comumente utilizados nas titulações de ácidos e bases, sejam fracos ou fortes. O indicador é um ácido ou uma base cujas espécies protonadas (ou desprotonadas) têm cores diferentes. Em solução aquosa, o comportamento de um indicador depende essencialmente do valor de pH.
28
Q826885
Julgue os itens de 101 a 106, relativos a ácidos e bases. Os ácidos fracos em solução aquosa não são completamente dissociados, mas os ácidos com constante de acidez (Ka) menor que 1 são completamente dissociados para todas as concentrações e podem ser considerados como ácidos fortes.
29
Q826884
Com relação à velocidade de reação química, a fatores que a influenciam e a assuntos correlatos, julgue os itens de 95 a 100. Catalisador é a substância ou espécie que aumenta a velocidade de reação, não é consumida e fornece um mecanismo alternativo de baixa energia de ativação para a reação. Um catalisador é capaz de afetar a constante de equilíbrio da reação considerada, por modificar a velocidade da reação direta, aumentando o tempo requerido para o estabelecimento do equilíbrio.
30
Q826883
Com relação à velocidade de reação química, a fatores que a influenciam e a assuntos correlatos, julgue os itens de 95 a 100. A velocidade de uma reação é proporcional às concentrações dos reagentes, com exceção das reações de ordem zero, em que as variações de concentração não produzem nenhum efeito.