 A tamisação é uma técnica de separação de mistura do tipo
A tamisação é uma técnica de separação de mistura do tipo  A tamisação é uma técnica de separação de mistura do tipo
A tamisação é uma técnica de separação de mistura do tipo 
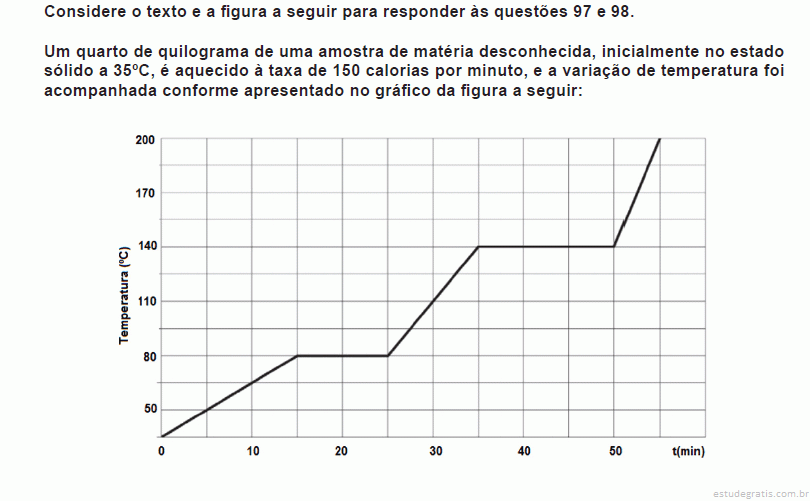

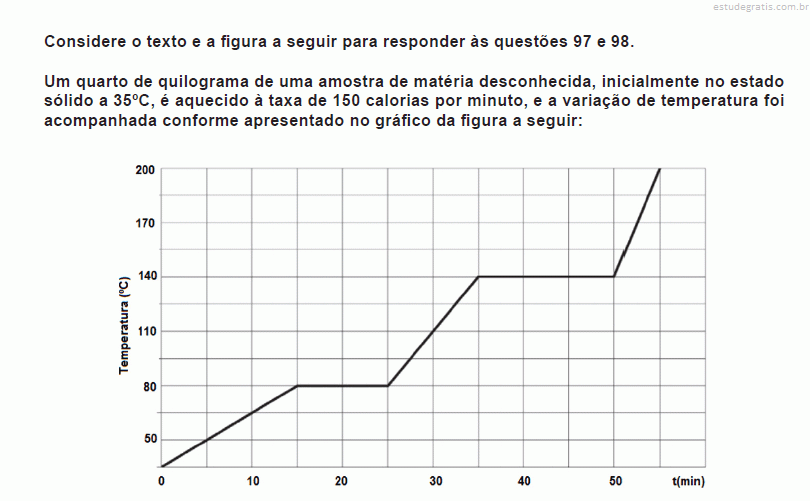

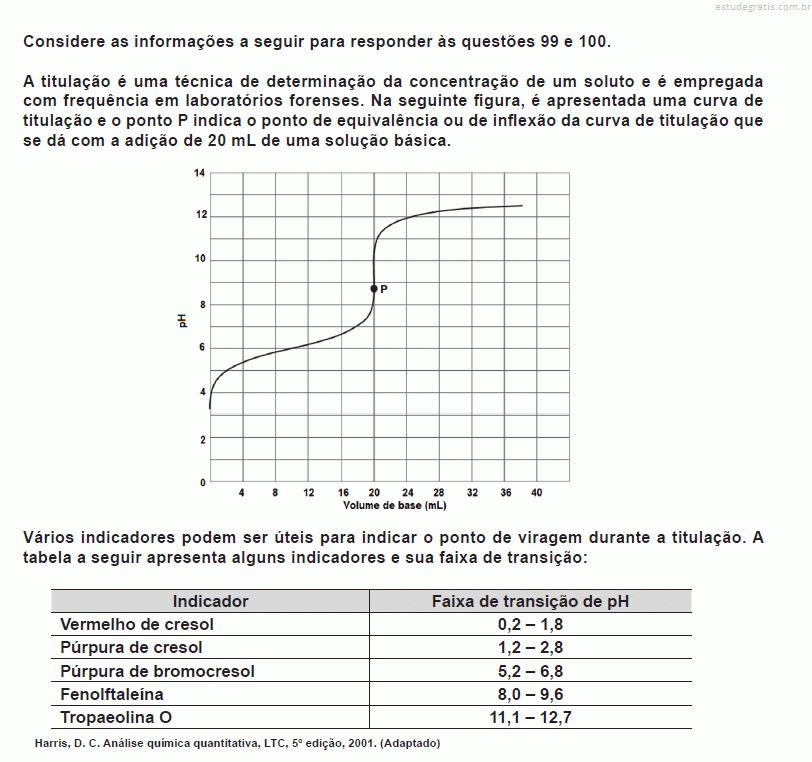

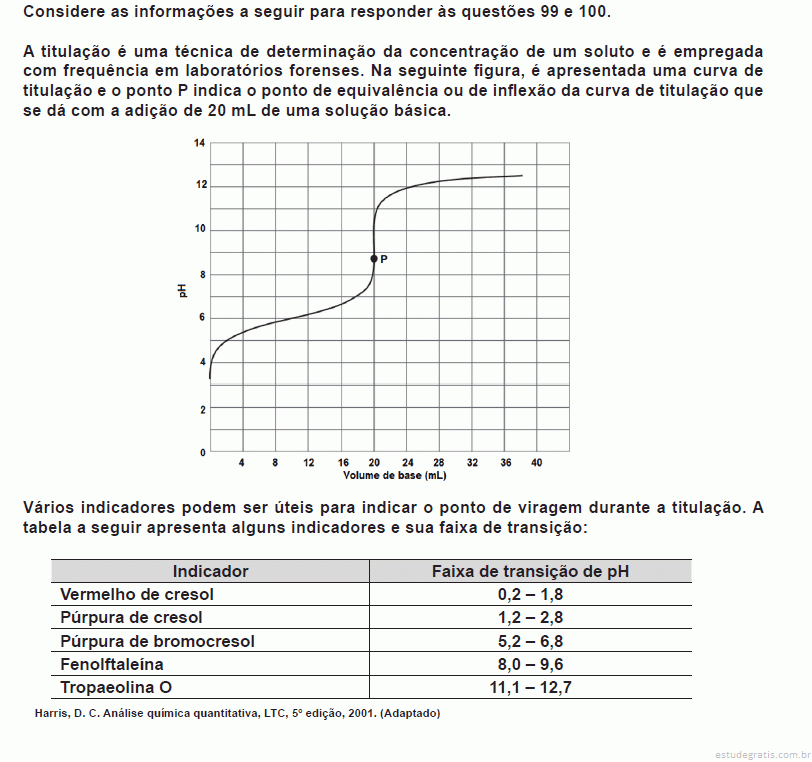
O pH ou potencial hidrogeniônico é uma escala logarítmica que mede o grau de acidez, neutralidade ou alcalinidade de uma determinada solução, compreendendo valores de 0 a 14, sendo que o 7 é considerado o valor neutro, o valor 0 (zero) representa a acidez máxima e o valor 14 a alcalinidade máxima.
No sistema de distribuição de água é recomendado que o pH seja mantido na faixa de
O iodeto de hidrogênio pode ser preparado a partir do hidrogênio e do iodo moleculares na fase gasosa, conforme equação a seguir.
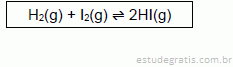
Em um dado momento, pode-se determinar o seu quociente de reação (Qc), que representa a razão das concentrações iniciais dos produtos e dos reagentes. Nessa reação, se o valor encontrado de Qc for menor que o valor da sua constante de equilíbrio (Kc), então,