A precipitação de cátions metálicos pela adição de um ânion com o qual eles formem composto insolúvel é uma ferramenta bastante utilizada para a remoção, identificação e(ou) quantificação de um metal em solução. Por exemplo, a adição de uma solução de H2S é empregada para promover a precipitação de sulfetos metálicos pouco solúveis.
Considerando que as constantes de ionização ácida do H2S (Ka1 e Ka2) sejam iguais a 1,0 × 10-7 e 1,0 × 10-13, que o produto de solubilidade (Kps) do CdS seja igual a 1,0 × 10-27 e que todas as soluções envolvidas apresentem comportamento ideal, julgue os itens a seguir.

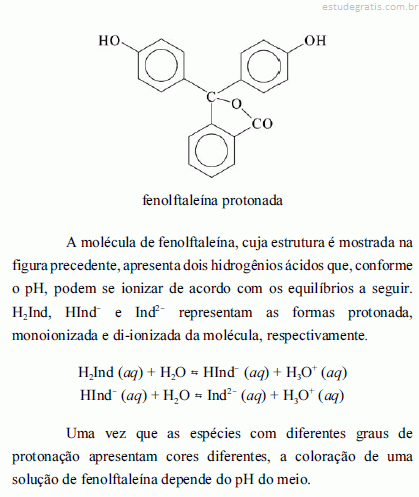
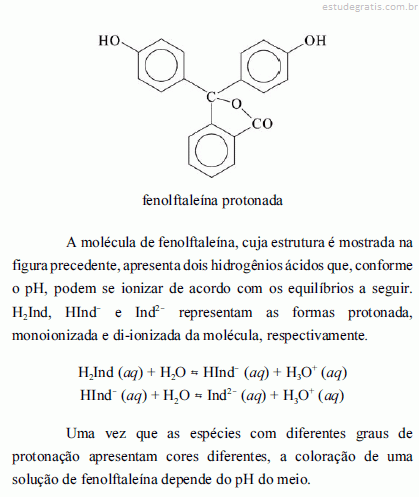
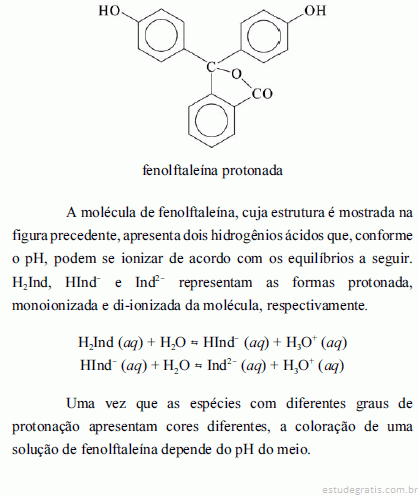
 A solubilidade de um sulfeto metálico é tanto menor quanto maior for a acidez do meio.
A solubilidade de um sulfeto metálico é tanto menor quanto maior for a acidez do meio.  Uma solução-tampão constituída por NH4Cl 0,040 mol/L e NH3 (aq) 0,030 mol/L apresenta pOH superior ao pKb da NH
Uma solução-tampão constituída por NH4Cl 0,040 mol/L e NH3 (aq) 0,030 mol/L apresenta pOH superior ao pKb da NH