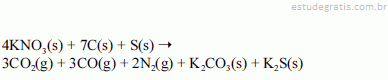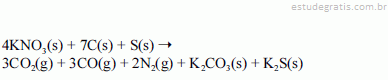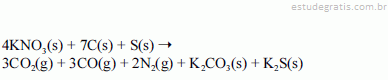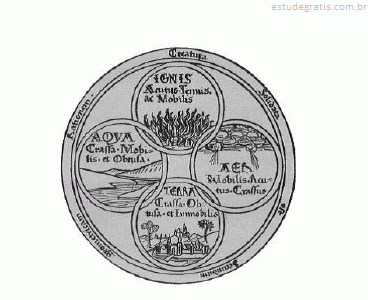
A figura precedente, que apresenta os quatro elementos da natureza (fogo, ar, terra e água), encontra-se no livro De responsione mundi et astrorum ordinatione — Augsburgo, 1472 —, obra baseada nos escritos de Santo Isidoro, bispo de Sevilha durante o século VII d.C., e representa símbolos da alquimia, pela qual vários materiais foram desenvolvidos empiricamente.
A pólvora é um desses materiais, e a compreensão do que ocorria na queima desse pó negro só aconteceu com a evolução da química moderna.
Considerando essas informações e os diversos aspectos a elas relacionados, julgue os itens que se seguem.
Algumas vidrarias, técni...