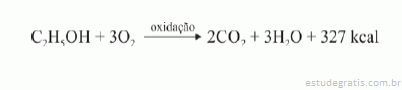
Sabendo que a reação apresentada mostra o processo de oxidação do etanol — em que são liberadas 327 kcal por mol de energia — e que as massas atômicas do carbono, do oxigênio e do hidrogênio são, respectivamente, iguais a 12, 16 e 1, julgue os itens a seguir.
A massa de 1 mol de etanol é 46 g.
Sabendo que a reação apresentada mostra o processo de oxidação do etanol — em que são liberadas 327 kcal por mol de energia — e que as massas atômicas do carbono, do oxigênio e do hidrogênio são, respectivamente, iguais a 12, 16 e 1, julgue os itens a seguir.
Para cada mol de etanol, são liberados 88 g de CO2.
Sabendo que a reação apresentada mostra o processo de oxidação do etanol — em que são liberadas 327 kcal por mol de energia — e que as massas atômicas do carbono, do oxigênio e do hidrogênio são, respectivamente, iguais a 12, 16 e 1, julgue os itens a seguir.
Para cada mol de etanol, a quantidade de O2 consumida é de 48 g.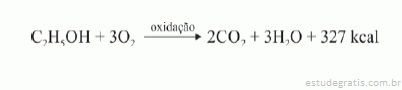
Sabendo que a reação apresentada mostra o processo de oxidação do etanol — em que são liberadas 327 kcal por mol de energia — e que as massas atômicas do carbono, do oxigênio e do hidrogênio são, respectivamente, iguais a 12, 16 e 1, julgue os itens a seguir.
Para cada mol de água produzido, a energia liberada é de 109 kcal.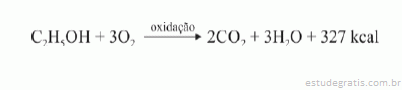
Sabendo que a reação apresentada mostra o processo de oxidação do etanol — em que são liberadas 327 kcal por mol de energia — e que as massas atômicas do carbono, do oxigênio e do hidrogênio são, respectivamente, iguais a 12, 16 e 1, julgue os itens a seguir.
Álcool etílico hidratado é uma mistura homogênea.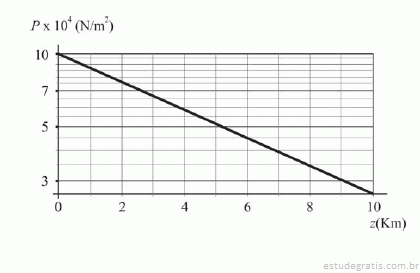
A figura precedente mostra um gráfico da pressão, em N/m2, em função da altura, em km, a partir do nível do mar. No gráfico, a pressão representada no eixo vertical está na escala logarítmica (ln); e a altura, no eixo horizontal, na escala linear. Para obter esse gráfico, a atmosfera foi considerada um gás ideal à temperatura constante. A partir dessas informações, julgue os itens seguintes.
A densidade da atmosfera, ρ, aumenta linearmente com a pressão, P, ou seja, ρ é proporcional à pressão.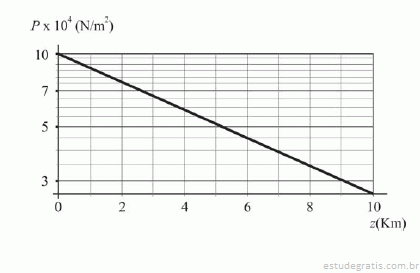
A figura precedente mostra um gráfico da pressão, em N/m2, em função da altura, em km, a partir do nível do mar. No gráfico, a pressão representada no eixo vertical está na escala logarítmica (ln); e a altura, no eixo horizontal, na escala linear. Para obter esse gráfico, a atmosfera foi considerada um gás ideal à temperatura constante. A partir dessas informações, julgue os itens seguintes.
A pressão atmosférica aumenta linearmente com a altura, ou seja, P é proporcional à altura z.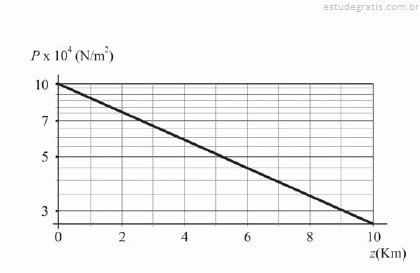
A figura precedente mostra um gráfico da pressão, em N/m2, em função da altura, em km, a partir do nível do mar. No gráfico, a pressão representada no eixo vertical está na escala logarítmica (ln); e a altura, no eixo horizontal, na escala linear. Para obter esse gráfico, a atmosfera foi considerada um gás ideal à temperatura constante. A partir dessas informações, julgue os itens seguintes.
A 4 km de altura, a pressão atmosférica é 40% do seu valor ao nível do mar.