Para uma amostra de solução desse ácido, o uso de um polarímetro permite determinar o ângulo de
21
Q848630
O ácido ricinoleico, um ácido graxo funcionalizado, cuja nomenclatura oficial é ácido D-(−)-12-hidroxioctadec-cis-9-enoico, é obtido da hidrólise ácida do óleo de mamona. As aplicações do ácido ricinoleico na indústria são inúmeras, podendo ser empregado desde a fabricação de cosméticos até a síntese de alguns polímeros.
Para uma amostra de solução desse ácido, o uso de um polarímetro permite determinar o ângulo de
Para uma amostra de solução desse ácido, o uso de um polarímetro permite determinar o ângulo de
22
Q848627
O 2-BHA é um fenol usado como antioxidante para retardar a rancificação em alimentos e cosméticos que contêm ácidos graxos insaturados. Esse composto caracteriza-se por apresentar uma cadeia carbônica aromática mononuclear, apresentando o grupo substituinte terc-butil na posição orto e o grupo metóxi na posição para.
A fórmula estrutural do fenol descrito é
A fórmula estrutural do fenol descrito é
23
Q848624
Na busca por ouro, os garimpeiros se confundem facilmente entre o ouro verdadeiro e o chamado ouro de tolo, que tem em sua composição 90% de um minério chamado pirita (FeS2). Apesar do engano, a pirita não é descartada, pois é utilizada na produção do ácido sulfúrico, que ocorre com rendimento global de 90%, conforme as equações químicas apresentadas. Considere as massas molares: FeS2 (120 g/mol) , O2 32 g/mol), Fe2O3 ( 160 g/mol) , SO2 ( 64 g/mol), SO3 ( 80 g/mol) , H2O ( 18 g/mol ) , H2SO4 ( 98 g/mol ).
4 FeS2 + 11 O2 →2 Fe2O3 + 8 SO2 2 SO2 + O2 →2 SO3 SO3 + H2O →H2SO4
Qual é o valor mais próximo da massa de ácido sulfúrico, em quilograma, que será produzida a partir de 2,0 kg de ouro de tolo?
4 FeS2 + 11 O2 →2 Fe2O3 + 8 SO2 2 SO2 + O2 →2 SO3 SO3 + H2O →H2SO4
Qual é o valor mais próximo da massa de ácido sulfúrico, em quilograma, que será produzida a partir de 2,0 kg de ouro de tolo?
24
Q848623
O etanol é um combustível renovável obtido da cana-de-açúcar e é menos poluente do que os combustíveis fósseis, como a gasolina e o diesel. O etanol tem densidade 0,8 g/cm3 , massa molar 46 g mol e calor de combustão aproximado de −1 300 kJ/mol . Com o grande aumento da frota de veículos, tem sido incentivada a produção de carros bicombustíveis econômicos, que são capazes de render até 20 km/L em rodovias, para diminuir a emissão de poluentes atmosféricos.
O valor correspondente à energia consumida para que o motorista de um carro econômico, movido a álcool, percorra 400 km na condição de máximo rendimento é mais próximo de
O valor correspondente à energia consumida para que o motorista de um carro econômico, movido a álcool, percorra 400 km na condição de máximo rendimento é mais próximo de
25
Q848621
O gás hidrogênio é considerado um ótimo combustível — o único produto da combustão desse gás é o vapor de água, como mostrado na equação química.
2 H2 (g) + O2 (g) → 2 H2O (g)
Um cilindro contém 1 kg de hidrogênio e todo esse gás foi queimado. Nessa reação, são rompidas e formadas ligações químicas que envolvem as energias listadas no quadro.
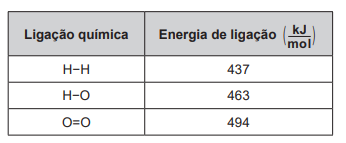
Massas molares ( g/mol ): H2 = 2; O2 = 32; H2O = 18.
Qual é a variação da entalpia, em quilojoule, da reação de combustão do hidrogênio contido no cilindro?
2 H2 (g) + O2 (g) → 2 H2O (g)
Um cilindro contém 1 kg de hidrogênio e todo esse gás foi queimado. Nessa reação, são rompidas e formadas ligações químicas que envolvem as energias listadas no quadro.

Massas molares ( g/mol ): H2 = 2; O2 = 32; H2O = 18.
Qual é a variação da entalpia, em quilojoule, da reação de combustão do hidrogênio contido no cilindro?
26
Q848619
Em 2014, iniciou-se em São Paulo uma séria crise hídrica que também afetou o setor energético, agravada pelo aumento do uso de ar-condicionado e ventiladores. Com isso, intensifica-se a discussão sobre a matriz energética adotada nas diversas regiões do país. Sendo assim, há necessidade de se buscarem fontes alternativas de energia renovável que impliquem menores impactos ambientais.
Considerando essas informações, qual fonte poderia ser utilizada?
Considerando essas informações, qual fonte poderia ser utilizada?
27
Q848618
Laboratórios de química geram como subprodutos substâncias ou misturas que, quando não têm mais utilidade nesses locais, são consideradas resíduos químicos. Para o descarte na rede de esgoto, o resíduo deve ser neutro, livre de solventes inflamáveis e elementos tóxicos como Pb, Cr e Hg. Uma possibilidade é fazer uma mistura de dois resíduos para obter um material que apresente as características necessárias para o descarte. Considere que um laboratório disponha de frascos de volumes iguais cheios dos resíduos, listados no quadro.
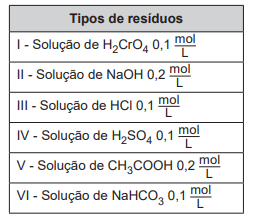
Qual combinação de resíduos poderá ser descartada na rede de esgotos?

Qual combinação de resíduos poderá ser descartada na rede de esgotos?
28
Q848615
O processo de calagem consiste na diminuição da acidez do solo usando compostos inorgânicos, sendo o mais usado o calcário dolomítico, que é constituído de carbonato de cálcio (CaCO3) e carbonato de magnésio (MgCO3). Além de aumentarem o pH do solo, esses compostos são fontes de cálcio e magnésio, nutrientes importantes para os vegetais.
Os compostos contidos no calcário dolomítico elevam o pH do solo, pois
Os compostos contidos no calcário dolomítico elevam o pH do solo, pois
29
Q848612
Nos municípios onde foi detectada a resistência do Aedes aegypti, o larvicida tradicional será substituído por outro com concentração de 10% (v/v) de um novo princípio ativo. A vantagem desse segundo larvicida é que uma pequena quantidade da emulsão apresenta alta capacidade de atuação, o que permitirá a condução de baixo volume de larvicida pelo agente de combate às endemias. Para evitar erros de manipulação, esse novo larvicida será fornecido em frascos plásticos e, para uso em campo, todo o seu conteúdo deve ser diluído em água até o volume final de um litro. O objetivo é obter uma concentração final de 2% em volume do princípio ativo.
Que volume de larvicida deve conter o frasco plástico?
Que volume de larvicida deve conter o frasco plástico?
30
Q848610
Antigamente, em lugares com invernos rigorosos, as pessoas acendiam fogueiras dentro de uma sala fechada para se aquecerem do frio. O risco no uso desse recurso ocorria quando as pessoas adormeciam antes de apagarem totalmente a fogueira, o que poderia levá-las a óbito, mesmo sem a ocorrência de incêndio.
A causa principal desse risco era o(a)
A causa principal desse risco era o(a)