Os seguintes dados foram anotados durante uma análise:
− Massa do cadinho vazio = 3,52 g.
− Massa do cadinho + amostra seca = 4,1008 g.
− Massa da amostra seca = X.
A massa, em gramas, que representa X corretamente é
Os seguintes dados foram anotados durante uma análise:
− Massa do cadinho vazio = 3,52 g.
− Massa do cadinho + amostra seca = 4,1008 g.
− Massa da amostra seca = X.
A massa, em gramas, que representa X corretamente é

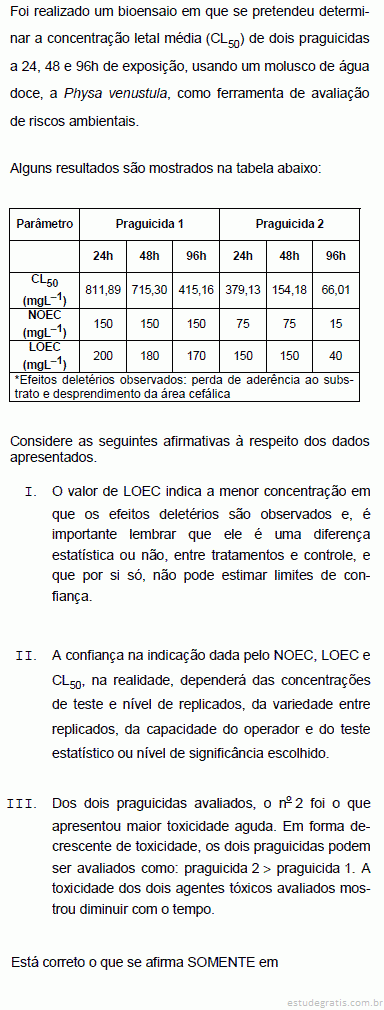
O IAP é o Índice para a determinação de qualidade das águas brutas para fins de abastecimento público. Ele é o produto da ponderação dos resultados do IQA (Índice de Qualidade de Águas) e do ISTO (Índice de Substâncias Tóxicas e Organolépticas). Por sua vez, o IQA comporta o grupo das variáveis básicas como Temperatura, pH, Oxigênio Dissolvido, Demanda Bioquímica de Oxigênio, Coliformes Termotolerantes, Nitrogênio Total, Fósforo Total, Resíduo Total e Turbidez. Já o ISTO, é composto por dois tipos de variáveis: o grupo de variáveis indicadoras de substâncias tóxicas, e o grupo de variáveis que afetam a qualidade organoléptica.
Dos itens abaixo, que são parâmetros observáveis dos grupos de variáveis que compõem o ISTO, quais pertenceriam ao grupo tóxi...
Dos processos abaixo, o único considerado endotérmico é a
O número de elétrons da camada de valência do átomo de fósforo no seu estado fundamental é
Dado: Número atômico do fósforo = 15Quando se compara o átomo neutro de ferro (Fe) com o íon Fe
3+
, ambos correspondentes ao isótopo de número de massa 56, observa-se que o íon possui três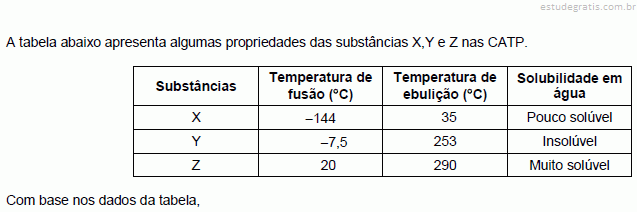
Três tubos de ensaio (I, II e III) contêm, cada um, 10 mililitros de água destilada a 25 °C. A esses tubos, foram adicionadas as seguintes massas de cloreto de sódio (NaCl):
Tubo I = 3,0 g Tubo II = 4,0 g Tubo III = 5,0 g
Sabendo-se que a solubilidade do NaCl a 25 °C é 36,0 g por 100 mL de água, após agitação, verificou-se existência de sólido e solução saturada em alguns tubos. O valor da massa de NaCl (s), em gramas, em cada um dos tubos I, II e III é, respectivamente,
William Justin Kroll, em 1946, mostrou que o titânio podia ser obtido comercialmente pela redução do TiCl4 com magnésio metálico. No processo Kroll, representado pela equação de óxido-redução não balanceada
TiCl4 + Mg → MgCl2 + Ti