Na espectroscopia de absorção atômica, a identificação e quantificação de determinado elemento é possível devido ao efeito da quantização da energia dos elétrons nos átomos, o qual faz com que os átomos apresentem linhas de absorção características de cada elemento. A figura a seguir apresenta a curva de calibração construída a partir de análises de espectroscopia de absorção atômica de soluções padrão de determinado metal. As absorbâncias correspondem a um comprimento de onda 8, sendo o caminho óptico percorrido pelo feixe de radiação através das soluções igual a 2,0 cm.
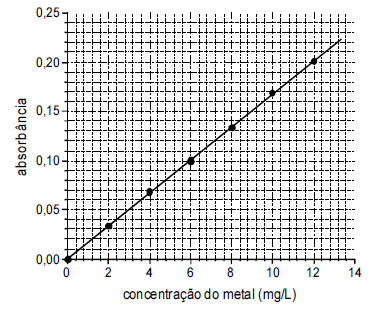
Considerando as informações fornecidas e a quantização de energia dos elétrons nos átomos, julgue ...
Na espectroscopia de absorção atômica, a identificação e quantificação de determinado elemento é possível devido ao efeito da quantização da energia dos elétrons nos átomos, o qual faz com que os átomos apresentem linhas de absorção características de cada elemento. A figura a seguir apresenta a curva de calibração construída a partir de análises de espectroscopia de absorção atômica de soluções padrão de determinado metal. As absorbâncias correspondem a um comprimento de onda 8, sendo o caminho óptico percorrido pelo feixe de radiação através das soluções igual a 2,0 cm.
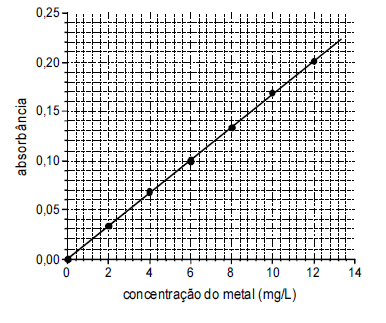
Considerando as informações fornecidas e a quantização de energia dos elétrons nos átomos, julgue ...
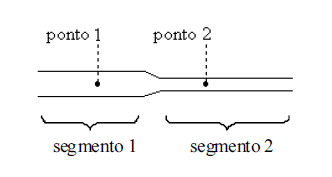
Considere que a tubulação acima representada é empregada para o transporte de um fluido. Para o segmento 1, o diâmetro do tubo é d; já para o segmento 2, o diâmetro é d/2.
Com relação a esse sistema, julgue o item subseqüente.
Para um fluido ideal, a velocidade v2 de escoamento no ponto 2 será duas vezes maior do que a velocidade de escoamento, v1, verificada no ponto 1.
Acerca do experimento acima descrito, julgue os itens que se seguem, considerando que M(H) = 1 g/mol; M(C) = 12 g/mol; M(O) = 16 g/mol; e M(Na) = 23 g/mol.
A massa de hidróxido de sódio presente em 250 mL da solução padronizada é igual a 1 g.
Acerca do experimento acima descrito, julgue os itens que se seguem, considerando que M(H) = 1 g/mol; M(C) = 12 g/mol; M(O) = 16 g/mol; e M(Na) = 23 g/mol.
A solução criada quando foram adicionados 20 mL de água no erlenmeyer deve apresentar um ponto de ebulição, à pressão de 1 atm, exatamente igual a 100 oC.
Acerca do experimento acima descrito, julgue os itens que se seguem, considerando que M(H) = 1 g/mol; M(C) = 12 g/mol; M(O) = 16 g/mol; e M(Na) = 23 g/mol.
O comprimido de analgésico sofreu liquefação quando foi adicionado água no erlenmeyer.
Acerca do experimento acima descrito, julgue os itens que se seguem, considerando que M(H) = 1 g/mol; M(C) = 12 g/mol; M(O) = 16 g/mol; e M(Na) = 23 g/mol.
Considere que, na solução padronizada de 0,1 mol/L de hidróxido de sódio, todo o soluto esteja completamente dissociado e não exista contaminantes. Nesse caso, em um litro dessa solução, estarão presentes 0,1 mol de Na+ e 0,1 mol de OH-.