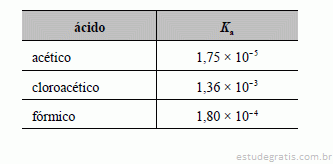
As figuras abaixo mostram dois cromatogramas obtidos por cromatografia líquida de alta eficiência (CLAE), sob condições idênticas, com exceção da composição da fase móvel. Para o cromatograma A, utilizou-se, para eluição, durante todo o procedimento, uma solução de acetonitrila em água na concentração de 70% em volume; e, para o cromatograma B, a solução utilizada foi de acetonitrila em água na concentração 60% em volume. Os parâmetros de polaridade da acetonitrila e da água usadas como fase móvel em cromatografia por partição são 5,8 e 10,2, respectivamente. O tempo de retenção do pico 1 pode ser considerado equivalente ao tempo médio que as moléculas da fase móvel permaneceram no interior da coluna.
...
 Para sistemas aquosos contendo impurezas metálicas, o valor de Kw, a 25 ºC, dependerá da natureza dessas impurezas, podendo ser maior ou menor que 1,0 × 10-14.
Para sistemas aquosos contendo impurezas metálicas, o valor de Kw, a 25 ºC, dependerá da natureza dessas impurezas, podendo ser maior ou menor que 1,0 × 10-14.  Para a água neutra, aquecida a 50 ºC, a concentração de íons hidrônio será maior que 1,0 ×10-7.
Para a água neutra, aquecida a 50 ºC, a concentração de íons hidrônio será maior que 1,0 ×10-7.