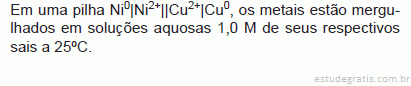
O valor da força eletromotriz (f.e.m) da pilha, em V, é

As baterias de Niquel-Cádmio são recarregáveis e bastante empregadas em aparelhos eletroeletrônicos, como filmadoras e máquinas fotográficas. Essas baterias são formadas por associações de duas ou mais pilhas. O eletrólito dessas pilhas consiste numa pasta de KOH. Nesse tipo de bateria,

As cores brilhantes observadas durante a queima de fogos de artifício são geradas a partir de elementos metálicos presentes nos fogos. Por exemplo, sais de estrôncio, como o SrCrO4, dão origem à luz vermelha; sais de cobre, como o Cu(NO3)2, à luz verde; sais de magnésio, como MgCl 2, à luz branca.
Sabendo que esse fenômeno pode ser explicado com base na estrutura eletrônica dos diferentes elementos metálicos, julgue os próximos itens.
No estado fundamental de energia, o íon Cu2+ apresenta 6 elétrons em orbitais s, 12 elétrons em orbitais p e 9 elétrons em orbitais d.Pilha de aeração diferencial é a pilha constituída de eletrodos de um só material metálico em contato com um mesmo eletrólito, mas apresentando regiões com diferentes teores de gases dissolvidos. Como ocorre com mais frequência em regiões diferentemente aeradas, é conhecida como o nome de pilha de aeração diferencial. (Considere: potencial padrão de redução é E° = 0,401 V.)
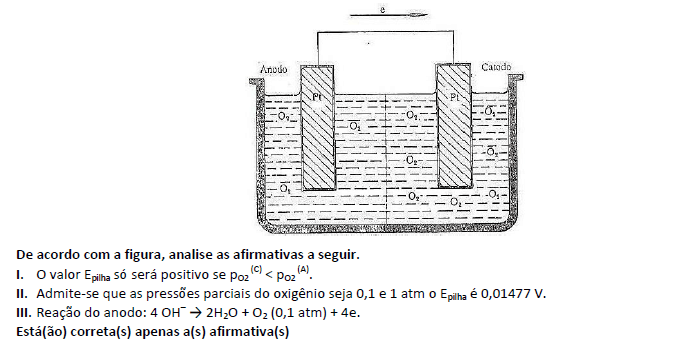
A teoria dos Orbitais Moleculares (MO) constitui uma alternativa para se ter uma visão da ligação. Os elétrons de valência têm uma influência na estabilidade da molécula. Sobre o tema, analise as afirmativas a seguir.
I. A teoria MO considera que os orbitais atômicos, AOs, da camada de valência, deixam de existir quando a molécula se forma, sendo substituídos por um novo conjunto de níveis energéticos que correspondem a novas distribuições da nuvem eletrônica.
II. Quando dois orbitais atômicos se combinam para formar dois orbitais moleculares, a energia de MO ligante é sempre maior do que a dos AOs, enquanto a energia do MO antiligante é menor.
III. A ordem de ligação na molécula de H2 é 1.
Está(ão) correta(s) apenas a(s) afirmativa(s)