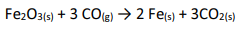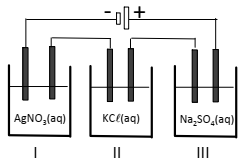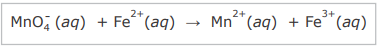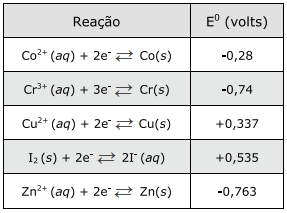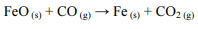
Caso essa reação seja realizada em etapas, as reações de cada etapa serão as seguintes, em que ?Hn (n = 1, 2 ou 3) representa a variação de entalpia da n-ésima etapa:

A partir da Lei de Hess, é possível calcular a variação de entalpia envolvida na pri...