As velocidades de reação independem do mecanismo da reação, pois independem do número de espécies colidindo. A expressão da constante de equilíbrio depende apenas da estequiometria, que descreve a relação entre as concentrações de reagentes e produtos quando o sistema atinge o estado de equilíbrio químico.
As velocidades de reação independem do mecanismo da reação, pois independem do número de espécies colidindo. A expressão da constante de equilíbrio depende apenas da estequiometria, que descreve a relação entre as concentrações de reagentes e produtos quando o sistema atinge o estado de equilíbrio químico.
S2O8 2 – (aq) + 3 I – (aq) ? 2 SO4 2 – (aq) + I3 – (aq)
A tabela a seguir contém dados experimentais sobre a reação em condições específicas de temperatura e pressão.
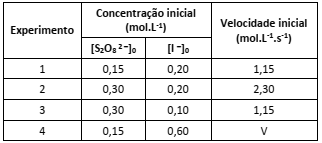
A partir das informações apresentadas é possível prever que a velocidade (V) do Experimento 4 será
A respeito de conceitos de química orgânica, julgue o próximo item.
A energia de ativação corresponde à energia que o sistema requer para ir dos reagentes até o estado de transição, sendo diretamente proporcional à velocidade do processo.
A respeito de conceitos de química orgânica, julgue o próximo item.
O aumento da concentração de um dos reagentes, em uma reação química, pode aumentar a velocidade da reação.


No ano de 2016 um novo sítio arqueológico foi descoberto no Brasil, na zona rural de São Manuel (SP), e pode representar um importante dado sobre a chegada dos humanos à América. Para estimar a idade dos objetos encontrados, amostras de carvão que estavam junto ao material foram enviadas para análise em laboratório nos EUA, que procedeu a datação por radiocarbono. Esse radioisótopo possui tempo de meia-vida de 5730 anos e, em uma fonte de material recente, ap...


Uma série de fatores alteram a velocidade de uma reação química. Observe a tabela a seguir, que mostra as condições iniciais usadas em três experimentos diferentes (I, II e III) envolvendo uma mesma reação com dois reagentes (A e B).

Os experimentos I, II e III, arrumados em ordem crescente de...
2 O3 (g) ? 3 O2 (g)
Uma proposta de mecanismo para essa reação é dada a seguir.I O3 (g) ? O2 (g) + O (g)
II O3 (g) + O (g) ? 2 O2 (g)
Com base nessas informações, julgue o próximo item.
Se a taxa de produção de oxigênio (d[O2]/dt) for igual a 3,0 × 10?5 mol/s, a taxa de consumo de ozônio (d[O3]/dt) será igual a ?2,0 × 10?5 mol/s.
2 O3 (g) ? 3 O2 (g)
Uma proposta de mecanismo para essa reação é dada a seguir.I O3 (g) ? O2 (g) + O (g)
II O3 (g) + O (g) ? 2 O2 (g)
Com base nessas informações, julgue o próximo item.
A reação da etapa II do mecanismo proposto ocorrerá se a energia potencial do complexo ativado for menor que a dos reagentes.
2 O3 (g) ? 3 O2 (g)
Uma proposta de mecanismo para essa reação é dada a seguir.I O3 (g) ? O2 (g) + O (g)
II O3 (g) + O (g) ? 2 O2 (g)
Com base nessas informações, julgue o próximo item.
A espécie O (g) é o catalisador da reação.
Com base nessas informações, julgue o próximo item.
A lei de velocidade de reações que ocorrem em muitas etapas é determinada pela reação global e, no caso da degradação do ozônio, ela é igual a ? = k [O3] 2 [O2] 3 , em que ? representa a velocidade da reação, k, a constante de velocidade e [O3] e [O2], as concentrações em quantidade de matéria de O3 e O2, respectivamente.