Acerca do equilíbrio em células galvânicas, julgue o próximo item.
Considera-se que o potencial produzido por uma célula galvânica seja a soma das contribuições do anodo e do catodo, ainda que o potencial de junção líquida seja considerável.
Acerca do equilíbrio em células galvânicas, julgue o próximo item.
Considera-se que o potencial produzido por uma célula galvânica seja a soma das contribuições do anodo e do catodo, ainda que o potencial de junção líquida seja considerável.
Julgue o item a seguir, referentes à cinética química, às leis de velocidade e à equação de Arrhenius.
Um processo elementar é aquele descrito por uma equação que especifica as quantidades de partículas do reagente e do produto envolvidas em dada etapa reacional.
Julgue o item a seguir, referentes à cinética química, às leis de velocidade e à equação de Arrhenius.
A energia de ativação para a reação de decomposição do dióxido de nitrogênio pode ser determinada a partir de um conjunto de experimentos em que se meça a taxa de reação a diferentes temperaturas.
Julgue o item a seguir, referentes à cinética química, às leis de velocidade e à equação de Arrhenius.
Define-se energia de ativação como a barreira energética que tem de ser suplantada pelos reagentes para iniciar-se uma reação, a qual será mais rápida quanto maior for a energia de ativação.
Julgue o item a seguir, referentes à cinética química, às leis de velocidade e à equação de Arrhenius.
O modelo de Arrhenius considera que a energia de ativação, a temperatura e a constante universal dos gases perfeitos são os únicos parâmetros que influenciam a constante cinética de uma reação.
Acerca de gases, julgue o item seguinte, considerando que o volume molar valha 22,4 L, que a constante universal dos gases perfeitos valha 62,4 L · mmHg · K?1 · mol?1 e que MH = 1 g/mol e MO = 16 g/mol.
A relação entre pressão e volume é norteada pela lei de Avogadro.
Acerca de gases, julgue o item seguinte, considerando que o volume molar valha 22,4 L, que a constante universal dos gases perfeitos valha 62,4 L · mmHg · K?1 · mol?1 e que MH = 1 g/mol e MO = 16 g/mol.
Nas condições normais de temperatura e pressão (CNTP), 180 g de água no estado de vapor ocupam um volume de 224 L.
Acerca de gases, julgue o item seguinte, considerando que o volume molar valha 22,4 L, que a constante universal dos gases perfeitos valha 62,4 L · mmHg · K?1 · mol?1 e que MH = 1 g/mol e MO = 16 g/mol.
Um gás cuja densidade seja de 1,26 g/L à temperatura de 50 ? e à pressão de 747 mmHg tem massa molar inferior a 35 g/mol.
Acerca de gases, julgue o item seguinte, considerando que o volume molar valha 22,4 L, que a constante universal dos gases perfeitos valha 62,4 L · mmHg · K?1 · mol?1 e que MH = 1 g/mol e MO = 16 g/mol.
A equação de Clapeyron pode ser utilizada para gases reais, desde que seja inserido fator de compressibilidade.
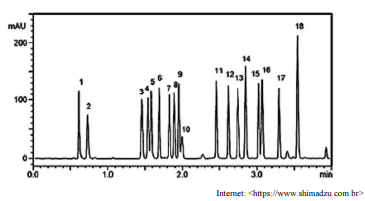
Entre as atividades desenvolvidas nos laboratórios da UnB, inclui-se a análise de aminoácidos (AAA). A figura precedente mostra um cromatograma de uma AAA obtido nas seguintes condições de análise.
• coluna: Shim-pack XR-ODS de fase reversa (3,0 mm d.i.; 75 mm)
• temperatura: 40 °C
• fase móvel: 10 mmol/L de fosfato de potássio (pH 7,0) e acetonitrila, eluição por gradiente
• fluxo: 1,2 mL/min
• detecção: 254 nm
...