61
Q826887
Julgue os itens de 101 a 106, relativos a ácidos e bases. A solução‐tampão é aquela cujo pH é mantido constante quando pequenas quantidades de ácido ou base são adicionadas. Um tampão básico, que estabiliza soluções em pH > 7, é preparado com uma solução que contém 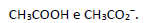
62
Q826886
Julgue os itens de 101 a 106, relativos a ácidos e bases. Indicadores ácido‐base são comumente utilizados nas titulações de ácidos e bases, sejam fracos ou fortes. O indicador é um ácido ou uma base cujas espécies protonadas (ou desprotonadas) têm cores diferentes. Em solução aquosa, o comportamento de um indicador depende essencialmente do valor de pH.
63
Q826885
Julgue os itens de 101 a 106, relativos a ácidos e bases. Os ácidos fracos em solução aquosa não são completamente dissociados, mas os ácidos com constante de acidez (Ka) menor que 1 são completamente dissociados para todas as concentrações e podem ser considerados como ácidos fortes.
64
Q826884
Com relação à velocidade de reação química, a fatores que a influenciam e a assuntos correlatos, julgue os itens de 95 a 100. Catalisador é a substância ou espécie que aumenta a velocidade de reação, não é consumida e fornece um mecanismo alternativo de baixa energia de ativação para a reação. Um catalisador é capaz de afetar a constante de equilíbrio da reação considerada, por modificar a velocidade da reação direta, aumentando o tempo requerido para o estabelecimento do equilíbrio.
65
Q826883
Com relação à velocidade de reação química, a fatores que a influenciam e a assuntos correlatos, julgue os itens de 95 a 100. A velocidade de uma reação é proporcional às concentrações dos reagentes, com exceção das reações de ordem zero, em que as variações de concentração não produzem nenhum efeito.
66
Q826882
No que se refere à termoquímica, a reações exotérmicas e endotérmicas e à variação de entalpia, julgue os itens de 89 a 94. Quando uma reação química se realiza à pressão constante, a quantidade de calor liberado ou absorvido é expressa pela variação da entalpia do sistema. Seu sinal algébrico indica se a reação é endotérmica ou exotérmica.
67
Q826881
A respeito de soluções e concentração de soluções, julgue os itens de 83 a 88. O tipo de composição porcentual de um reagente sempre deve estar especificado explicitamente. O erro potencial resultante de uma opção incorreta é considerável. Por exemplo, para uma solução de hidróxido de sódio comercial a 50% (m/m), sua concentração corresponde a 50% (m/v) de hidróxido de sódio.
68
Q826880
A respeito de soluções e concentração de soluções, julgue os itens de 83 a 88. As três formas de expressar a concentração em termos de porcentagem, a saber, porcentual em massa, porcentual em volume e porcentual em massa/volume, apresentam a característica de serem independentes da temperatura.
69
Q826879
A respeito de soluções e concentração de soluções, julgue os itens de 83 a 88. O porcentual em massa/volume é geralmente utilizado para indicar a composição de soluções aquosas diluídas de reagentes sólidos. Desse modo, o nitrato de potássio a 5% aquoso normalmente se refere a uma solução preparada pela solubilização de 5 g de KNO3 em água suficiente para perfazer 100 mL de solução.
70
Q826878
A respeito de soluções e concentração de soluções, julgue os itens de 83 a 88. Em termos de porcentual em massa, um reagente aquoso comercializado como uma solução a 70% contém 70 g de reagente para cada 100 g de solvente.