221
Q634011
Acerca da segunda lei da termodinâmica, de entropia e de espontaneidade de reações, assinale a opção correta.
222
Q634010
Acerca da Lei de Hess e de entalpias de formação, assinale a opção correta.
223
Q634009
Com relação à variação de entropia (ΔS) e à variação da energia livre de Gibbs (ΔG), assinale a opção correta.
224
Q634008
Considerando que a constante universal dos gases seja 8,31451 kPaLK-1mol-1, o valor da pressão exercido por 5,6 g de nitrogênio gasoso em um frasco de volume igual a 200 mL, a 20 ºC, em quilopascal (kPa) é
225
Q634007
A respeito das propriedades dos gases, assinale a opção correta.
226
Q634006
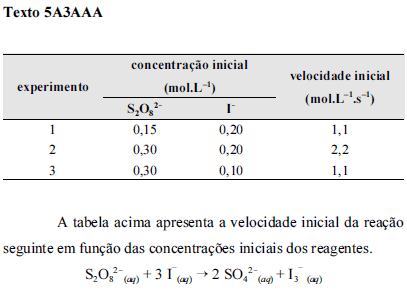
Considerando-se que k seja a constante de velocidade da reação apresentada no texto 5A3AAA, é correto afirmar que a lei de velocidade para essa reação é
227
Q634005
A relação correta entre as taxas de variações das concentrações das espécies envolvidas na reação apresentada no texto 5A3AAA, desconsiderando a ocorrência de intermediários, é
228
Q634004
A respeito da reação elementar 2A (g) 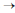 produto, assinale a opção correta.
produto, assinale a opção correta.
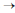 produto, assinale a opção correta.
produto, assinale a opção correta.
229
Q634003
Ainda em relação à reação elementar 2A (g)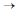 produto, assinale a opção cujo gráfico representa o comportamento da concentração da espécie reagente A em função do tempo.
produto, assinale a opção cujo gráfico representa o comportamento da concentração da espécie reagente A em função do tempo.
 produto, assinale a opção cujo gráfico representa o comportamento da concentração da espécie reagente A em função do tempo.
produto, assinale a opção cujo gráfico representa o comportamento da concentração da espécie reagente A em função do tempo.
230
Q634002
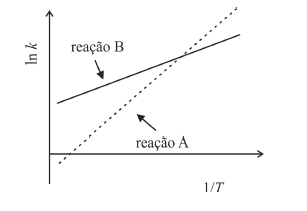
A partir da equação de Arrhenius e do gráfico precedente, correspondente ao logaritmo neperiano da constante de velocidade (k) em função do inverso da temperatura (T), em graus kelvin, para as reações A e B, é correto afirmar que a reação A apresenta energia de ativação