501
Q445481
O processo de tratamento biológico de um efluente doméstico pode ser aeróbico ou anaeróbico. Além da diferença na quantidade de lodo produzido, o processo anaeróbico apresenta a
502
Q445479

503
Q445478
Algumas substâncias orgânicas são um desafio à depuração biológica, já que o nível de biodegradação é extremamente baixo ou nulo, e ainda muitas vezes acabam prejudicando a decomposição de outros poluentes associados. Para romper as estruturas desses compostos orgânicos devem ser usados processos
504
Q445476
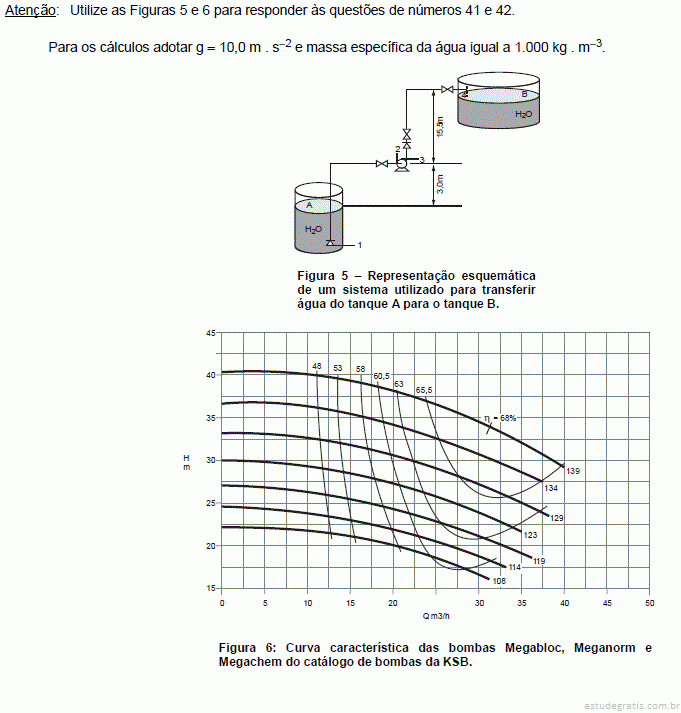 Admitindo-se a pressão de vapor da água igual a 10.000 Pa e a pressão atmosférica de 100.000 Pa, o NPSH disponível ou altura manométrica disponível na sucção da bomba é de:
Admitindo-se a pressão de vapor da água igual a 10.000 Pa e a pressão atmosférica de 100.000 Pa, o NPSH disponível ou altura manométrica disponível na sucção da bomba é de:
505
Q445474
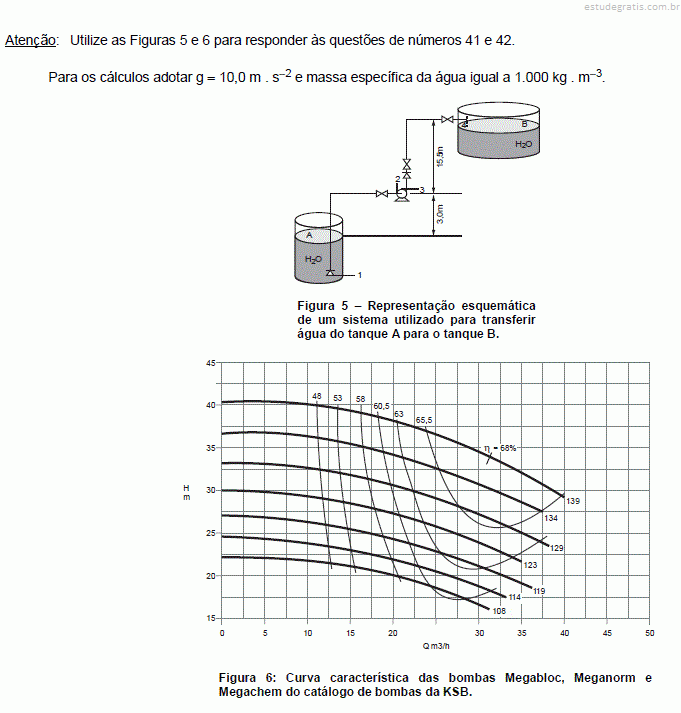
Na instalação da Figura 5 deseja-se bombear água a 20 °C na vazão de 30 m3 . h−1. A perda de carga na tubulação na sucção (trecho 1 a 2) é de 10,0 J . kg−1. Já a perda de carga na tubulação no recalque (trecho 3 a 4) é de 3,0 m.c.a. Será utilizado a bomba KSB Megabloc modelo 32-125 com rotação de 3.500 rpm, no gráfico a altura manométrica (H) é dada em m.c.a., a vazão da água (Q) em m3 . h−1 e os diâmetros dos rotores em mm. Desprezar a variação de energia cinética.
O menor diâmetro do rotor que atenderá a instalação é de
506
Q445472
A dureza da água afeta a formação de espuma e produz incrustações nos sistemas que envolvem o aquecimento de água. Essa dureza se deve
507
Q445470
Reatores de manta de lodo ou Upflow Anaerobic Sludge Blanket − UASB também chamados de Reator Anaeróbico de Fluxo Ascendente − RAFA são compostos por:
508
Q445469
Trata-se de uma tecnologia capaz de separar desde sólidos em suspensão até elementos iônicos. Permite inclusive a reciclagem de águas e efluentes líquidos para finalidades de reuso mais nobres. A tecnologia em questão é a de
509
Q445467

510
Q445465
Um efluente contendo ácido sulfúrico (H2SO4) com uma concentração de 0,10 mol . L−1 de solução será neutralizado com uma solução de hidróxido de sódio (NaOH) a 4,0 mol . L−1 de solução. O tratamento é em batelada e o volume de efluente ácido a tratar é de 20,0 m3. O volume necessário de hidróxido de sódio na concentração de 4,0 mol . L−1 é de