Uma solução de HCl foi padronizada empregando um padrão primário de Na2CO3 previamente seco em estufa por 24 horas a 110°C. Foi pesado 0,2500 g deste padrão primário e transferido para um erlenmeyer de 250 mL, sendo dissolvidos com 50 mL de água destilada e adicionadas 3 gotas de indicador alaranjado de metila. Após colocar a solução de HCl na bureta, efetuou-se a titulação, adicionando-se o ácido à solução de Na2CO3 até o ponto de viragem do indicador, cor amarela. O volume de HCl consumido foi igual a 25,00 mL. Suponha que as pesagens do padrão primário e as titulações foram feitas em triplicata e foram alcançados os mesmos valores nos três casos. Assinale a alternativa que apresenta a concentração molar aproximada do HCl que deve ser encontrada após os cálculos.
...Uma amostra de 25 mL de uma solução aquosa de H2SO4 foi titulada com uma solução aquosa 0,10 mol/L de KOH. Determinou-se que o volume da base necessário para atingir a viragem do indicador foi igual a 20 mL. Suponha que as titulações foram feitas em triplicata e todas forneceram os mesmos resultados. Assinale a concentração, em mol/L, de H2SO4 na solução ácida.
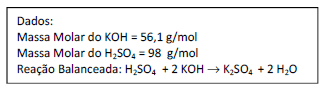
A respeito do conceito de pressão de vapor, analise as seguintes situações.
I - Em uma cidade como Poços de Caldas, localizada a 1.196 metros acima do nível do mar, a temperatura de ebulição da água, em panela aberta, é superior a 100 °C como consequência da pressão atmosférica em Poços de Caldas ser maior que ao nível do mar.
II - Na panela de pressão fechada, a água entra em ebulição acima de 100 °C graças à retenção de parte do vapor produzido, que gera aumento da pressão interna.
III - Considerando três frascos iguais e fechados, numa mesma localidade, contendo volumes diferentes de água e todos mantidos à mesma temperatura, a pressão de vapor de água nos três frascos será a mesma em todos eles, desde que a quantidade de líquido colocada em cada um seja ...
Dada a seguinte reação:

Assinale a variação de entalpia, em kJ/mol, dessa reação.
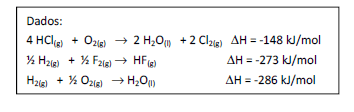
A entalpia-padrão de combustão do etanol líquido é -1367 kJ/mol e sua densidade é 0,80 g/mL. A energia liberada na queima de 1 litro de etanol, em kJ/mol, bem como a quantidade, em quilogramas, de CO2 liberados na atmosfera, respectivamente, serão aproximadamente:

Sobre os fatores que influenciam na velocidade de reações químicas, marque V para as afirmativas verdadeiras e F para as falsas.
( ) Quanto maior for a concentração dos reagentes, maior será a velocidade de reação.
( ) Colisões efetivas nem sempre levam à formação de novos produtos.
( ) Quanto maior a energia de ativação, mais rápida será a reação.
( ) Quanto maior a temperatura, maior será a velocidade de uma reação.
Assinale a sequência correta.
A respeito de lei de velocidade de reações químicas, observe a reação abaixo e os dados obtidos experimentalmente.

Marque a alternativa que apresenta a lei de velocidade que concorda com os dados experimentais.

Verificando a intensidade de mudança de cor na solução por um sensor embutido no equipamento, pode-se estimar a quantidade de álcool presente no sangue do motorista. O limite atual é 0,05 miligramas por litro de ar expirado. Nesse caso, a variação no número de oxidação do átomo de cromo presente nos íons dessa reação é igual a: