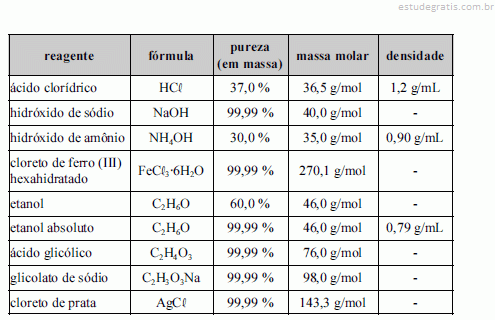
A tabela acima apresenta reagentes utilizados para o preparo de algumas soluções. Com base nessas informações, julgue os itens a seguir.
O pH de uma solução obtida pela mistura de 50 mL de NaOH 0,1 mol/L e 50 mL de HCR 0,25 mol/L é inferior a 2.
A tabela acima apresenta reagentes utilizados para o preparo de algumas soluções. Com base nessas informações, julgue os itens a seguir.
O pH de uma solução obtida pela mistura de 50 mL de NaOH 0,1 mol/L e 50 mL de HCR 0,25 mol/L é inferior a 2.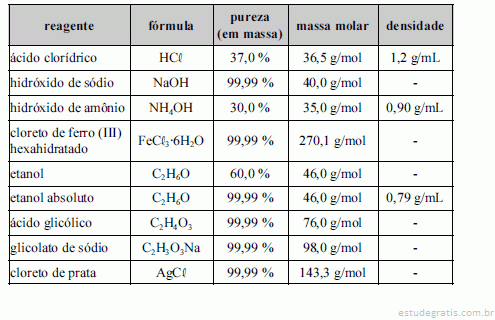
A tabela acima apresenta reagentes utilizados para o preparo de algumas soluções. Com base nessas informações, julgue os itens a seguir.
Para se preparar 1,0 L de uma solução aquosa 0,1 mol/L de Fe3+ são necessários 10,8 g do reagente FeCl 3·6H2O.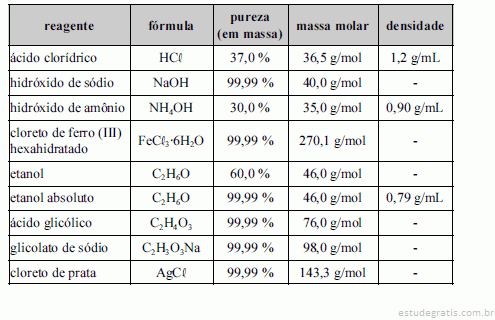
A tabela acima apresenta reagentes utilizados para o preparo de algumas soluções. Com base nessas informações, julgue os itens a seguir.
Em 500 mL de uma solução de NaOH 0,2 mol/L, a massa de NaOH contida é maior que 5,0 g.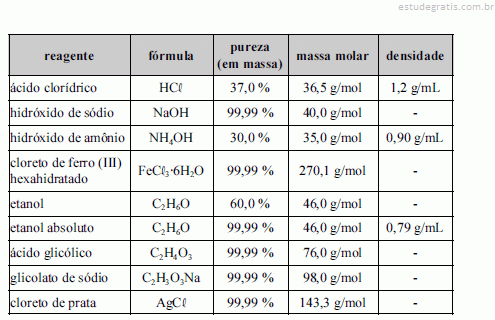
A tabela acima apresenta reagentes utilizados para o preparo de algumas soluções. Com base nessas informações, julgue os itens a seguir.
A mistura de 100 mL de etanol a 60,0 % com 100 mL de etanol absoluto produz uma solução final de concentração superior a 75,0 % em massa.Considere as situações I e II a seguir.
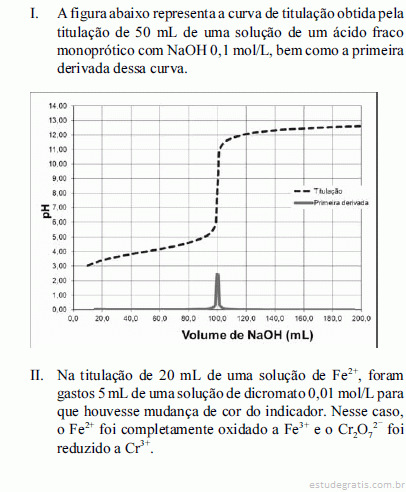
Com base nas situações apresentadas acima, julgue os itens a seguir, relativos à química analítica clássica.
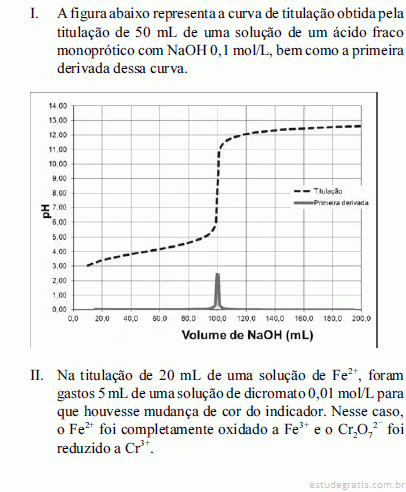
Na situação I, a concentração do ácido titulado é o dobro da concentração da base utilizada nessa titulação.Considere as situações I e II a seguir.
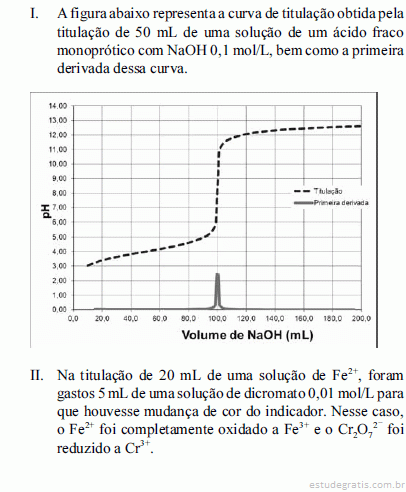
Com base nas situações apresentadas acima, julgue os itens a seguir, relativos à química analítica clássica.
O ácido titulado na situação I é mais forte que o ácido propiônico, que tem pKa = 4,9.Considere as situações I e II a seguir.
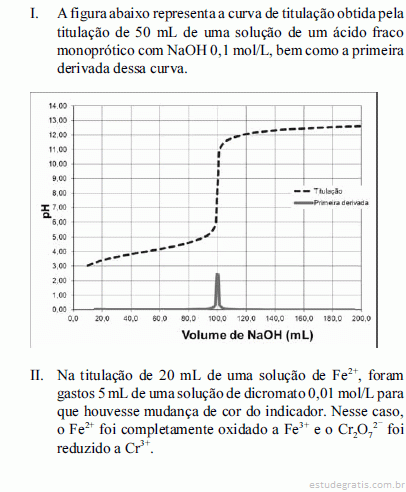
Com base nas situações apresentadas acima, julgue os itens a seguir, relativos à química analítica clássica.
Na situação II, a concentração de Fe2+ na amostra é superior a 0,010 mol/L.Considere as situações I e II a seguir.
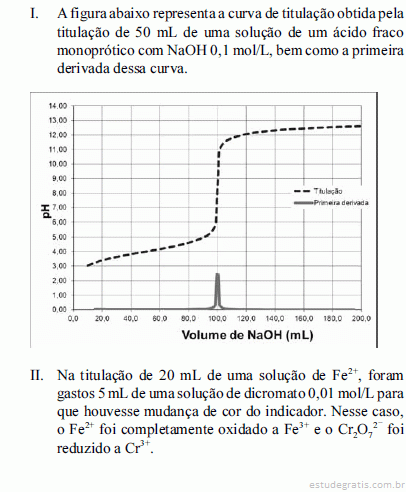
Com base nas situações apresentadas acima, julgue os itens a seguir, relativos à química analítica clássica.
Uma maneira de eliminar os erros aleatórios relativos às medidas de volume durante a titulação na situação II é a utilização de uma bureta eletrônica no lugar da vidraria convencional.Considere as situações I e II a seguir.
Com base nas situações apresentadas acima, julgue os itens a seguir, relativos à química analítica clássica.
Em uma titulação de neutralização, caso a adição do indicador gere uma solução de coloração muito escura, aconselha-se adicionar água ao titulado para que a coloração fique mais clara, o que torna mais precisa e exata a detecção do ponto final da titulação.