As cores brilhantes observadas durante a queima de fogos de artifício são geradas a partir de elementos metálicos presentes nos fogos. Por exemplo, sais de estrôncio, como o SrCrO4, dão origem à luz vermelha; sais de cobre, como o Cu(NO3)2, à luz verde; sais de magnésio, como MgCl 2, à luz branca.
Sabendo que esse fenômeno pode ser explicado com base na estrutura eletrônica dos diferentes elementos metálicos, julgue os próximos itens.
De acordo com o modelo atômico de Rutherford-Bohr, quando aquecidos, diferentes elementos químicos geram diferentes cores porque emitem radiação contínua.Na figura a seguir é apresentado de modo esquemático, as formas de diversos orbitais moleculares obtidos por combinações lineares de orbitais atômicos. O eixo z é, normalmente, tomado como eixo internuclear.
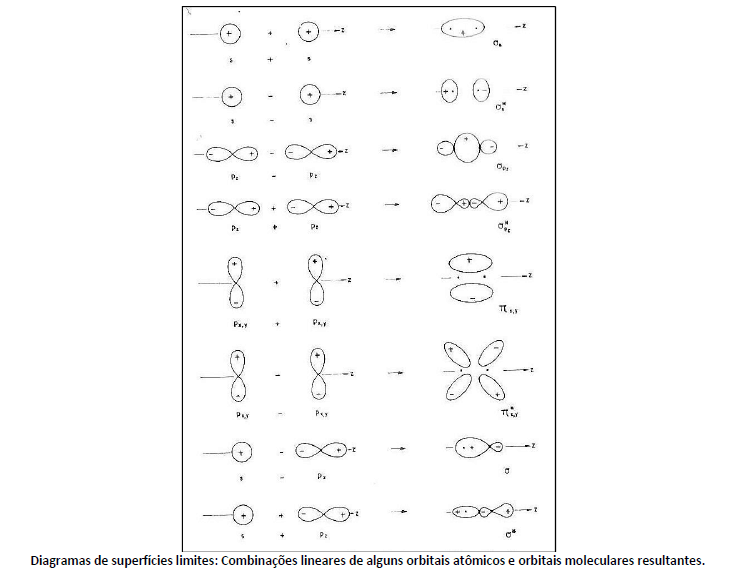
Sobre a figura, analise as afirmativas a seguir.
I. As regiões nodais já existentes nos OAs persistem nos OMs.
II. Toda vez que há uma região nodal, a função de ondas não muda de sinal.
III. Qualquer orbital molecular antiligante possui um plano nodal perpendicular ao eixo internuclear e situado entre os núcleos.
Está(ão) correta(s) apenas a(s) afirmativa(s)

Tendo o texto acima como referência, julgue os próximos itens.
Considere o postulado da teoria atômica de Dalton que institui que, em determinado composto, os números relativos de átomos de um certo tipo são definidos e constantes. Esse postulado não permite justificar a formação das moléculas H2O e H2O2, por determinar que dois elementos podem formar apenas um composto.
Considerando o texto acima, julgue os itens seguintes.
A radiação gama citada no texto é um fenômeno originado na eletrosfera dos átomos.