...
1
Q1134543
Pelo modelo atômico de ________________, o átomo é constituído por um núcleo central dotado de cargas eletricamente positivas (prótons) e onde está praticamente concentrada toda a massa do átomo, envolvido por uma nuvem contendo partículas de carga negativas (elétrons). Esse modelo poderia ser comparado ao nosso sistema solar: o núcleo sendo representado pelo sol, e os planetas representando os elétrons, como representado na Figura 1 a seguir:
...
...
2
Q1129955
A ideia de que os elétrons ocupam níveis de energia específicos ao redor do núcleo atômico, podendo absorver ou emitir energia ao se deslocarem entre essas órbitas bem definidas, é uma característica do modelo atômico de:
3
Q1127824
Os modelos atômicos são teorias que tentam explicar a matéria e seus fenômenos. Eles foram evoluindo com o tempo, de acordo com os avanços da ciência. Analise as afirmativas a seguir:
I. John Dalton propôs em sua teoria que átomos de elementos diferentes apresentam massas diferentes.
II. O modelo atômico inicialmente proposto por Rutherford apresentava o átomo contendo a eletrosfera situada ao redor do núcleo, composto por prótons e nêutrons.
III. O modelo atômico de Thomson apresenta o átomo contendo partículas negativas incrustadas em uma esfera positiva.
VI. No modelo atômico proposto por John Dalton, o átomo, apesar de ser uma esfera maciça, poderia ser divido em partes menores.
V. De acordo com a teoria atômica de Rutherford, pode-...
I. John Dalton propôs em sua teoria que átomos de elementos diferentes apresentam massas diferentes.
II. O modelo atômico inicialmente proposto por Rutherford apresentava o átomo contendo a eletrosfera situada ao redor do núcleo, composto por prótons e nêutrons.
III. O modelo atômico de Thomson apresenta o átomo contendo partículas negativas incrustadas em uma esfera positiva.
VI. No modelo atômico proposto por John Dalton, o átomo, apesar de ser uma esfera maciça, poderia ser divido em partes menores.
V. De acordo com a teoria atômica de Rutherford, pode-...
4
Q1124809
Sobre os modelos atômicos e a estrutura do átomo, analise as assertivas abaixo:
I. O modelo de Dalton descrevia o átomo como uma esfera maciça, indivisível e sem carga elétrica.
II. O modelo de Thomson propôs a existência de partículas subatômicas, descrevendo o átomo como uma esfera positiva com elétrons distribuídos em seu interior.
III. Rutherford, com seu experimento da folha de ouro, demonstrou que o átomo possui um núcleo pequeno, denso e carregado positivamente, rodeado por elétrons em órbitas circulares fixas.
IV. O modelo de Bohr introduziu a ideia de que os elétrons giram em órbitas quantizadas ao redor do núcleo, podendo saltar entre níveis de energia mediante absorção ou emissão de energia.
V. O modelo mecânico-quântico desc...
I. O modelo de Dalton descrevia o átomo como uma esfera maciça, indivisível e sem carga elétrica.
II. O modelo de Thomson propôs a existência de partículas subatômicas, descrevendo o átomo como uma esfera positiva com elétrons distribuídos em seu interior.
III. Rutherford, com seu experimento da folha de ouro, demonstrou que o átomo possui um núcleo pequeno, denso e carregado positivamente, rodeado por elétrons em órbitas circulares fixas.
IV. O modelo de Bohr introduziu a ideia de que os elétrons giram em órbitas quantizadas ao redor do núcleo, podendo saltar entre níveis de energia mediante absorção ou emissão de energia.
V. O modelo mecânico-quântico desc...
5
Q1098150
Um estudante leu as seguintes descrições sobre um conjunto de elementos químicos:
• Gás nobre de menor número atômico;
• Metal alcalino terroso de maior número atômico;
• Calcogênio de menor número atômico.
Ao identificar os elementos químicos, o estudante encontrará como resposta os símbolos dos elementos químicos, na ordem:
• Gás nobre de menor número atômico;
• Metal alcalino terroso de maior número atômico;
• Calcogênio de menor número atômico.
Ao identificar os elementos químicos, o estudante encontrará como resposta os símbolos dos elementos químicos, na ordem:
6
Q952304
O avanço da tecnologia nos levou a tecnologias como o LED (diodos emissores de luz) ou laser. Esses esforços foram conseguidos graças ao aperfeiçoamento dos modelos atômicos, principalmente ao modelo atômico oriundo da mecânica quântica. Porém, mesmo distante em suas concepções, os modelos atômicos de Bohr e o modelo quântico possuem semelhanças. Sob essa perspectiva, analise as afirmativas a seguir.
I. Em ambos os modelos, os elétrons encontram-se em órbitas circulares, em um raio fixo. II. Ambos os modelos, os elétrons são vistos como ondas, ao invés de partículas. III. Em ambos os modelos, a energia de um elétron é quantizada, ou seja, ele pode receber ou emitir determinados valores "permitidos". IV. No modelo de Bohr, o elétron é visto como partícula, no modelo quântico, como on...
I. Em ambos os modelos, os elétrons encontram-se em órbitas circulares, em um raio fixo. II. Ambos os modelos, os elétrons são vistos como ondas, ao invés de partículas. III. Em ambos os modelos, a energia de um elétron é quantizada, ou seja, ele pode receber ou emitir determinados valores "permitidos". IV. No modelo de Bohr, o elétron é visto como partícula, no modelo quântico, como on...
7
Q951844
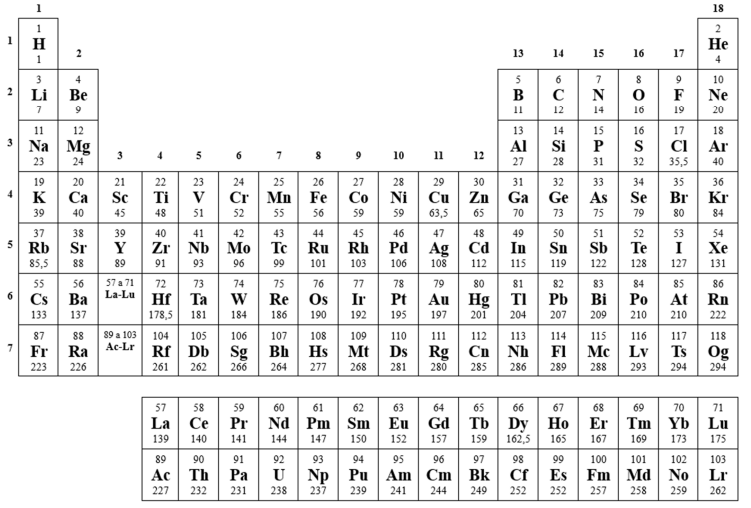
Numere a coluna da direita de acordo com a da esquerda, associando os exemplos à classe de compostos.
(1) Ácido de Lewis ( ) NH3
(2) Base de Arrhenius ( ) CH3COOH
(3) Base fraca de Bronsted-Lowry ( ) KNO3
(4) Ácido forte de Bronsted-Lowry ( ) HCl
(5) Componente ácido de tampão ( ) NH4Cl
(6) Componente salino de tampão ácido ( ) BF3
(7) Sal ácido ( ) CH3COONa
(8) Sal neutro ...
8
Q951403
Do que são formadas as coisas? Essa é uma das questões mais antigas da humanidade e várias hipóteses foram levantadas para tentar respondê-la.
Considerando o texto apresentado, avalie as proposições a seguir:
I- Modelo bola de bilhar: Dalton teve a ideia de que deveria ser algo maciço muito pequeno e indivisível, chamado de átomo.
II- Modelo pudim de passas: Thompson identificou partículas negativas, denominadas de elétrons, e supôs que também deveria haver prótons.
III- Modelo Rutherford-Bohr: Rutherford determinou que o átomo é formado por duas regiões (o núcleo e a eletrosfera) e Bohr inferiu que havia neutros permitindo que houvesse um espaço entre as camadas de elétrons dos átomos.
É CORRETO o que se afirma em:
Considerando o texto apresentado, avalie as proposições a seguir:
I- Modelo bola de bilhar: Dalton teve a ideia de que deveria ser algo maciço muito pequeno e indivisível, chamado de átomo.
II- Modelo pudim de passas: Thompson identificou partículas negativas, denominadas de elétrons, e supôs que também deveria haver prótons.
III- Modelo Rutherford-Bohr: Rutherford determinou que o átomo é formado por duas regiões (o núcleo e a eletrosfera) e Bohr inferiu que havia neutros permitindo que houvesse um espaço entre as camadas de elétrons dos átomos.
É CORRETO o que se afirma em:
9
Q951161
Acerca da natureza elétrica da matéria, julgue o próximo item.
Conforme o modelo atômico de Dalton, também conhecido como modelo pudim de passas, o átomo é tal qual uma esfera de material gelatinoso com carga positiva sobre a qual os elétrons ficam suspensos.
10
Q1060320
Julgue o item seguinte, relativos às propriedades periódicas.
A energia de ionização é aquela liberada quando um átomo isolado no estado fundamental, em fase gasosa, recebe um elétron.