431
Q937615
Diversos modelos atômicos foram formulados para compreender os átomos e os seus comportamentos. O número de prótons, nêutrons e elétrons de cada espécie é um fator determinante para sua caracterização elementar. O número de massa e o número de prótons de um determinado elemento pode ser informado por pXA , onde p é o número de prótons, A é a massa atômica e x um elemento químico. De acordo com seus conhecimentos sobre estrutura atômica, assinale a alternativa correta.
432
Q937614
A tabela periódica é um arranjo de forma a organizar os elementos químicos conhecidos de acordo com seu número atômico, distribuição eletrônica e propriedades periódicas, que são propriedades que seguem uma lógica de ordenamento de acordo com as colunas e linhas das tabelas periódicas. De acordo com seus conhecimentos sobre propriedades periódicas, assinale a alternativa correta.
433
Q937613
Reações de neutralização são reações entre um ácido e uma base que produzem sal e água, de acordo com os conceitos de Arrhenius. O sal inorgânico formado é então um produto iônico dessa reação que ao ter contato com a água é dissolvido liberando no mínimo um cátion diferente de H+ e no mínimo um ânion diferente de OH-. Considerando a dissolução de um sal em uma solução aquosa neutra, assinale a alternativa correta.
434
Q937612
O iodeto de potássio (KI) é uma substância aplicada como fonte de iodo, uma vez que se trata de um sal cristalino menos higroscópio que outros compostos, como o iodeto de sódio (NaI). Uma via para obtenção do iodeto de potássio (KI) é a redução do iodato de potássio (KIO3) por carbono com formação de dióxido de carbono nos produtos. Supondo-se que deseja-se produzir 166 g de iodeto de potássio por redução de carbono, a quantidade dos reagentes, iodato de potássio e carbono, em gramas, é, respectivamente
Pesos moleculares: I=127 g/mol; K= 39 g/mol; O= 16 g/mol; C=12 g/mol.
Pesos moleculares: I=127 g/mol; K= 39 g/mol; O= 16 g/mol; C=12 g/mol.
435
Q937611
Sobre os procedimentos de saúde e segurança que devem ser adotados em laboratório, assinale a alternativa correta.
436
Q937610
Considere o seguinte ciclo de uma máquina térmica descrito e representado na figura abaixo para responder a questão. Um litro de 0,04 mols de um gás ideal a um atm de pressão no ponto 1 é submetido a um aquecimento isovolumétrico até o ponto 2, aumentando 30% sua pressão. Em seguida é realizada uma compressão isotérmica até o ponto 3. Posteriormente, o gás sofre uma expansão adiabática até o ponto 1. Considere que todos os processos ocorrem reversivelmente.
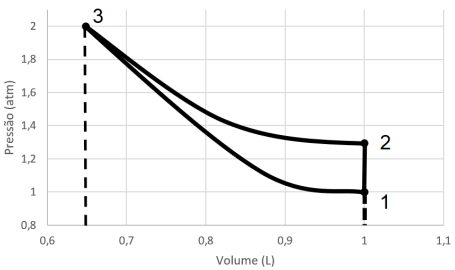
Assinale a alternativa correta sobre o ciclo descrito.

Assinale a alternativa correta sobre o ciclo descrito.
437
Q937609
Sabendo que a constante universal dos gases é de 0,082 atm.L.K-1.mol-1, calcule a temperatura do ponto 1 e do ponto 2.
438
Q937608
Considere as três afirmativas a seguir sobre o ciclo apresentado anteriormente:
I. A variação de entropia ao longo do ciclo é nula. II. A variação de trabalho ao longo do ciclo é nula. III. A variação de energia interna ao longo do ciclo é nula.
Assinale
I. A variação de entropia ao longo do ciclo é nula. II. A variação de trabalho ao longo do ciclo é nula. III. A variação de energia interna ao longo do ciclo é nula.
Assinale
439
Q937607
Considere o diagrama binário de um sistema líquido-vapor que mostra a influência da fração do soluto a (xa) em função da temperatura (T) para responder a questão.
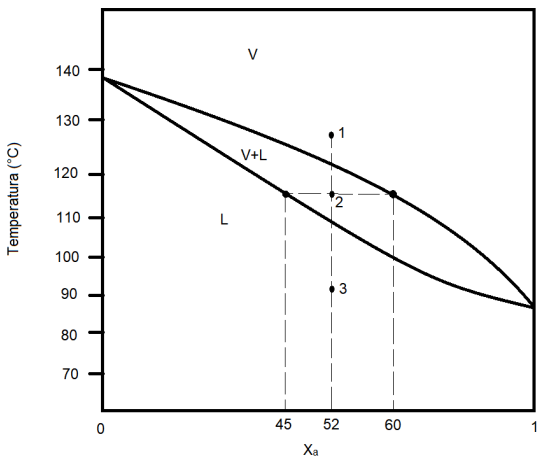
Assinale a alternativa correta a respeito do resfriamento de uma mistura do ponto 1 até o ponto 3.

Assinale a alternativa correta a respeito do resfriamento de uma mistura do ponto 1 até o ponto 3.
440
Q937606
Considerando o ponto 2 do diagrama, assinale a alternativa que apresenta corretamente a fração de líquido e o teor do soluto B presente no vapor, respectivamente.