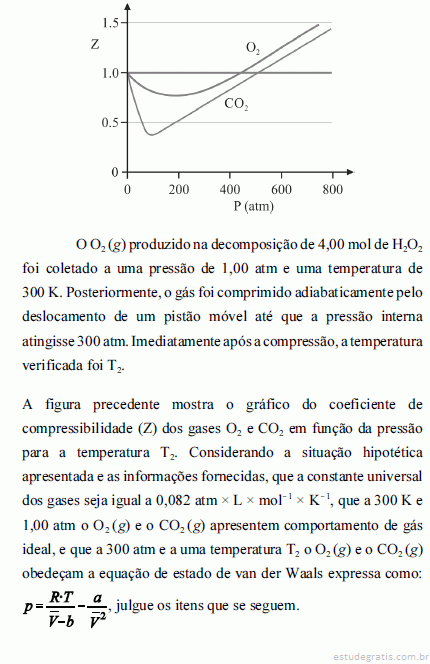
 Quando atingida a pressão de 300 atm e a temperatura T2, o volume ocupado pelo gás será menor do que aquele que seria ocupado, nas mesmas condições, por um gás ideal.
Quando atingida a pressão de 300 atm e a temperatura T2, o volume ocupado pelo gás será menor do que aquele que seria ocupado, nas mesmas condições, por um gás ideal.  Quando atingida a pressão de 300 atm e a temperatura T2, o volume ocupado pelo gás será menor do que aquele que seria ocupado, nas mesmas condições, por um gás ideal.
Quando atingida a pressão de 300 atm e a temperatura T2, o volume ocupado pelo gás será menor do que aquele que seria ocupado, nas mesmas condições, por um gás ideal. 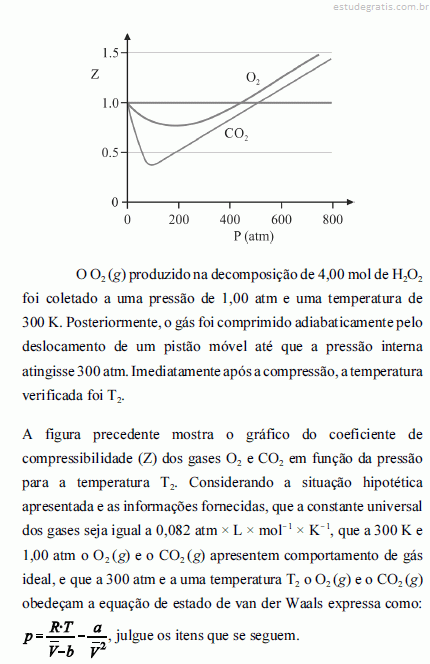 A temperatura T2 é inferior àquela verificada imediatamente antes da compressão.
A temperatura T2 é inferior àquela verificada imediatamente antes da compressão. 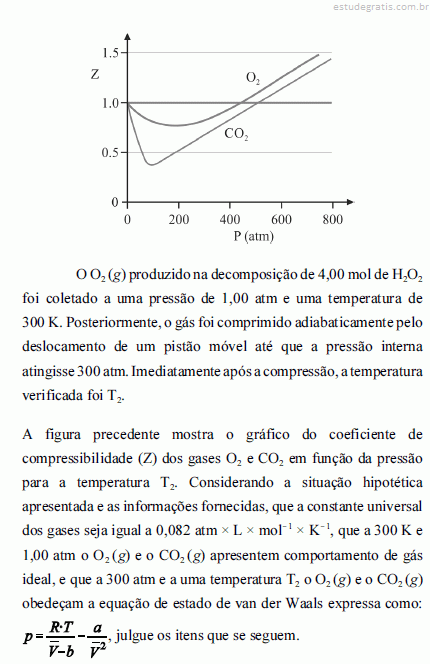 A uma pressão de 1,00 atm e temperatura de 300 K, o volume ocupado pelo O2 (g) formado na decomposição de 4,00 mol de H2O2 será superior a 46,0 L.
A uma pressão de 1,00 atm e temperatura de 300 K, o volume ocupado pelo O2 (g) formado na decomposição de 4,00 mol de H2O2 será superior a 46,0 L. 
Considerando que a reação de decomposição do H2O2 seja exotérmica e se processe de acordo com uma cinética de primeira ordem, e que a constante universal dos gases seja igual a 8,3 J × mol-1 × K-1, julgue os itens subsequentes, acerca da reação em questão.
As entalpias padrão de ligação fornecidas permitem determinar que a decomposição de 1,00 mol de H2O2, quando realizada à pressão constante de 1 bar e a 25 ºC, libera quantidade de calor superior a 100 kJ.
Considerando que a reação de decomposição do H2O2 seja exotérmica e se processe de acordo com uma cinética de primeira ordem, e que a constante universal dos gases seja igual a 8,3 J × mol-1 × K-1, julgue os itens subsequentes, acerca da reação em questão.
A reação de decomposição do H2O2 libera maior quantidade de calor quando é realizada à pressão constante de 1 bar do que quando é realizada a volume constante.
Considerando que a reação de decomposição do H2O2 seja exotérmica e se processe de acordo com uma cinética de primeira ordem, e que a constante universal dos gases seja igual a 8,3 J × mol-1 × K-1, julgue os itens subsequentes, acerca da reação em questão.
Em temperaturas mais elevadas, o valor da constante de equilíbrio da reação de decomposição do H2O2 é superior ao verificado em temperaturas mais baixas.
Considerando que a reação de decomposição do H2O2 seja exotérmica e se processe de acordo com uma cinética de primeira ordem, e que a constante universal dos gases seja igual a 8,3 J × mol-1 × K-1, julgue os itens subsequentes, acerca da reação em questão.
O fato de a reação de decomposição do H2O2 ser de primeira ordem implica tratar-se de uma reação elementar.
Considerando que a reação de decomposição do H2O2 seja exotérmica e se processe de acordo com uma cinética de primeira ordem, e que a constante universal dos gases seja igual a 8,3 J × mol-1 × K-1, julgue os itens subsequentes, acerca da reação em questão.
O tempo necessário para que a concentração de H2O2 caia a 10% do valor inicial equivale a 10 × ek, em que k é a constante de velocidade da reação de decomposição do H2O2.
Considerando que a reação de decomposição do H2O2 seja exotérmica e se processe de acordo com uma cinética de primeira ordem, e que a constante universal dos gases seja igual a 8,3 J × mol-1 × K-1, julgue os itens subsequentes, acerca da reação em questão.
A curva resultante da plotagem do logaritmo neperiano da concentração do H2O2 em função do tempo de reação resulta em uma reta com inclinação negativa.
Considerando que a reação de decomposição do H2O2 seja exotérmica e se processe de acordo com uma cinética de primeira ordem, e que a constante universal dos gases seja igual a 8,3 J × mol-1 × K-1, julgue os itens subsequentes, acerca da reação em questão.
A partir do gráfico apresentado e de acordo com a equação de Arrhenius, é possível determinar que a energia de ativação da reação é superior a 1,0 × 105 J × mol-1.