Questão
Q952286
Prova: IBFC - 2023 - Prefeitura de Cuiabá - MT - Químico
•
Prefeitura de Cuiabá - MT
Um químico preparou uma solução de Ba+2 comconcentraçã
Um químico preparou uma solução de Ba+2 comconcentração 0,025M. Inicia-se então umatitulação com 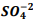 seguindo a reação: B?SO4(s) ?
seguindo a reação: B?SO4(s) ? 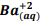 +
+ 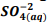 , onde Kps = [ B?+2] [
, onde Kps = [ B?+2] [ 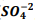 ] = 1, 1 x10?10. Verifica-se que:
] = 1, 1 x10?10. Verifica-se que:
I. A partir da concentração de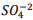 acima de0,025M inicia a precipitação de Ba+2. II. Em concentrações menores que 4,4 x10?9 M jáhouve precipitação de B?SO4.
acima de0,025M inicia a precipitação de Ba+2. II. Em concentrações menores que 4,4 x10?9 M jáhouve precipitação de B?SO4.
Assinale a alternativa correta:
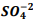 seguindo a reação: B?SO4(s) ?
seguindo a reação: B?SO4(s) ? 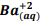 +
+ 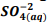 , onde Kps = [ B?+2] [
, onde Kps = [ B?+2] [ 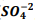 ] = 1, 1 x10?10. Verifica-se que:
] = 1, 1 x10?10. Verifica-se que: I. A partir da concentração de
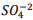 acima de0,025M inicia a precipitação de Ba+2. II. Em concentrações menores que 4,4 x10?9 M jáhouve precipitação de B?SO4.
acima de0,025M inicia a precipitação de Ba+2. II. Em concentrações menores que 4,4 x10?9 M jáhouve precipitação de B?SO4. Assinale a alternativa correta:
Comentários
Faça login para participar da discussão.
Cadastre-se Gratuitamente
Carregando comentários...