
Considerando que as reações de hidrogenação sejam exotérmicas, que todos os gases envolvidos apresentem comportamento ideal e que o produto da constante universal dos gases pela temperatura absoluta (R×T) seja igual a 2.500 J/mol, julgue os itens que se seguem.
Considere que a reação de hidrogenação em apreço seja de ordem um com relação ao C2H4 (g) e de ordem um com relação ao H2 (g), e que as concentrações iniciais de cada um dos dois reagentes sejam iguais a x0. Nessas condições, a concentração de C2H4 em um instante t da reação é dada por x0/(1 + k’.t.x0), em que k’ é a constante de velocidade na temperatura da reação.
Considerando que as reações de hidrogenação sejam exotérmicas, que todos os gases envolvidos apresentem comportamento ideal e que o produto da constante universal dos gases pela temperatura absoluta (R×T) seja igual a 2.500 J/mol, julgue os itens que se seguem.
A energia de ativação da reação de hidrogenação catalisada pelo metal B é superior à da reação catalisada pelo metal A.
Considerando que as reações de hidrogenação sejam exotérmicas, que todos os gases envolvidos apresentem comportamento ideal e que o produto da constante universal dos gases pela temperatura absoluta (R×T) seja igual a 2.500 J/mol, julgue os itens que se seguem.
Sob determinada temperatura, a reação de hidrogenação do C2H4 (g) liberará maior quantidade de calor se realizada a volume constante, e não a pressão constante.
Considerando que as reações de hidrogenação sejam exotérmicas, que todos os gases envolvidos apresentem comportamento ideal e que o produto da constante universal dos gases pela temperatura absoluta (R×T) seja igual a 2.500 J/mol, julgue os itens que se seguem.
A constante de equilíbrio para a reação de hidrogenação do C2H4 (g) a 100 ºC é maior que a 25 ºC.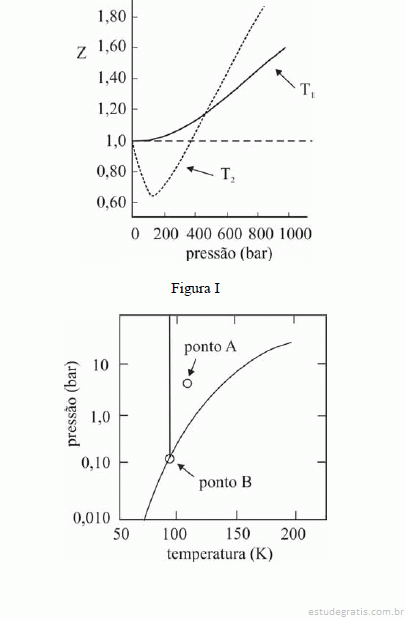
A figura I ilustra o gráfico do coeficiente de compressibilidade (Z) do CH4 (g) em função da pressão para duas temperaturas distintas (T1 e T2), e a figura II representa o diagrama de fases desse mesmo composto. A partir das figuras apresentadas, julgue os itens que se seguem.
Na temperatura e pressão correspondentes ao ponto A da figura II, o potencial químico do metano gasoso é superior ao do metano líquido.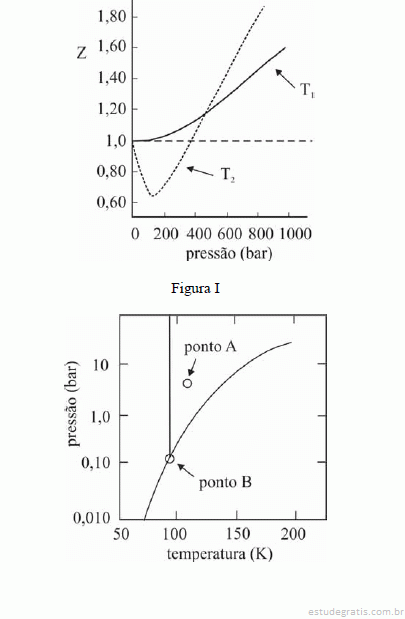
A figura I ilustra o gráfico do coeficiente de compressibilidade (Z) do CH4 (g) em função da pressão para duas temperaturas distintas (T1 e T2), e a figura II representa o diagrama de fases desse mesmo composto. A partir das figuras apresentadas, julgue os itens que se seguem.
O CH4 não pode ser liquefeito por simples compressão à temperatura de 150 K, uma vez que o ponto B, na figura II, corresponde à temperatura crítica desse gás.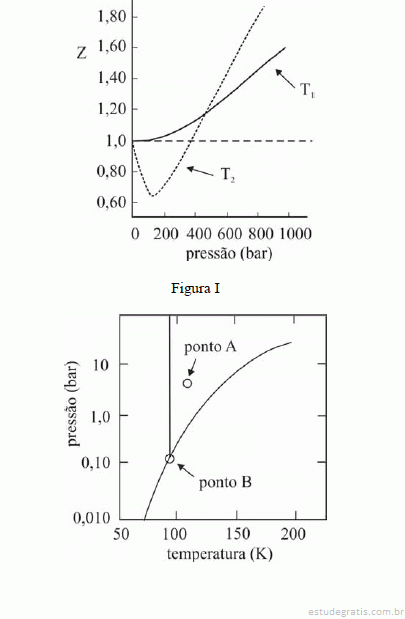
A figura I ilustra o gráfico do coeficiente de compressibilidade (Z) do CH4 (g) em função da pressão para duas temperaturas distintas (T1 e T2), e a figura II representa o diagrama de fases desse mesmo composto. A partir das figuras apresentadas, julgue os itens que se seguem.
Infere-se da situação mostrada na figura I que T1 é maior que T2.