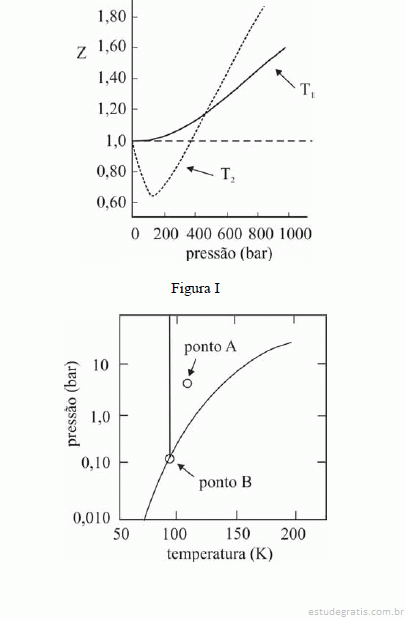
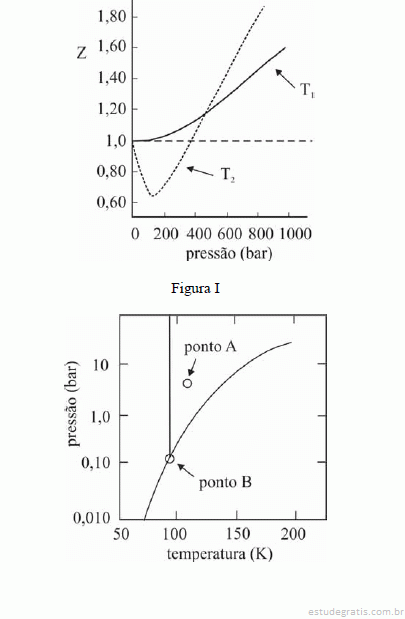
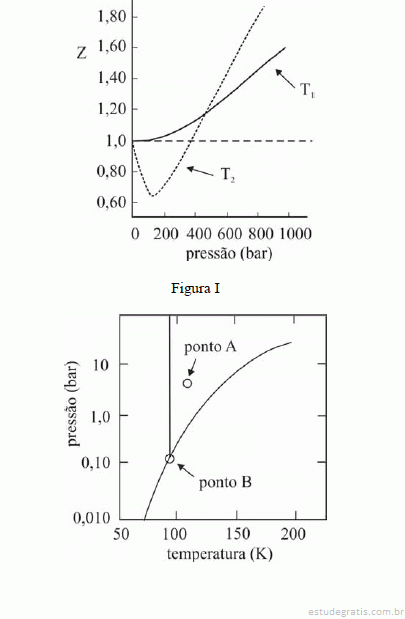
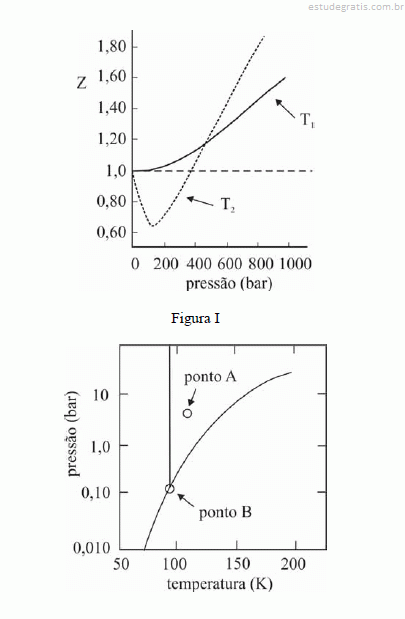
Considerando que as reações de hidrogenação sejam exotérmicas, que todos os gases envolvidos apresentem comportamento ideal e que o produto da constante universal dos gases pela temperatura absoluta (R×T) seja igual a 2.500 J/mol, julgue os itens que se seguem.
Considere que a reação de hidrogenação em apreço seja de ordem um com relação ao C2H4 (g) e de ordem um com relação ao H2 (g), e que as concentrações iniciais de cada um dos dois reagentes sejam iguais a x0. Nessas condições, a concentração de C2H4 em um instante t da reação é dada por x0/(1 + k’.t.x0), em que k’ é a constante de velocidade na temperatura da reação.