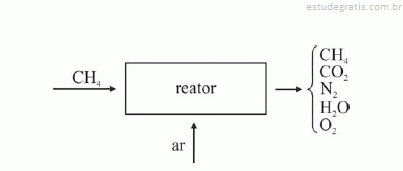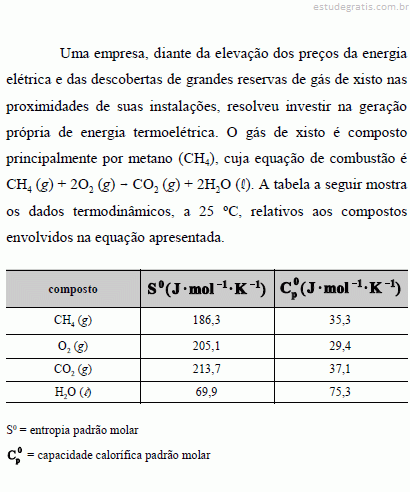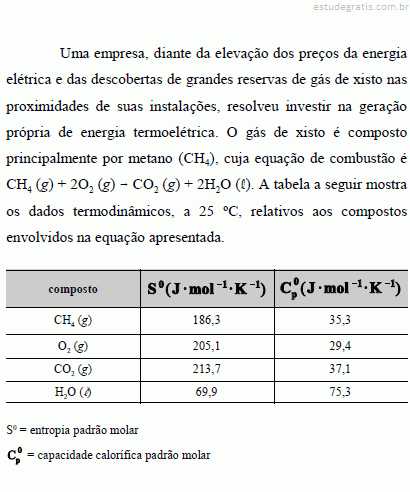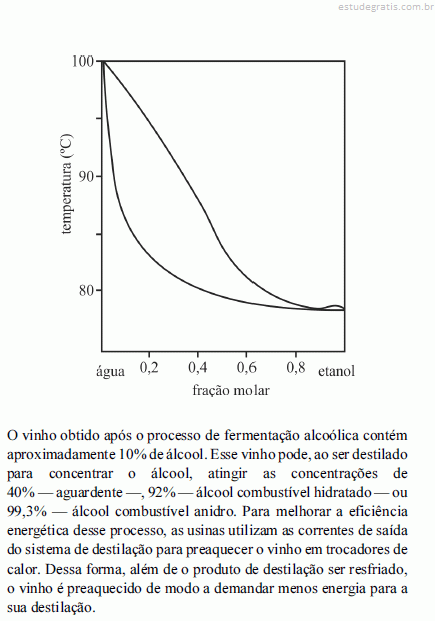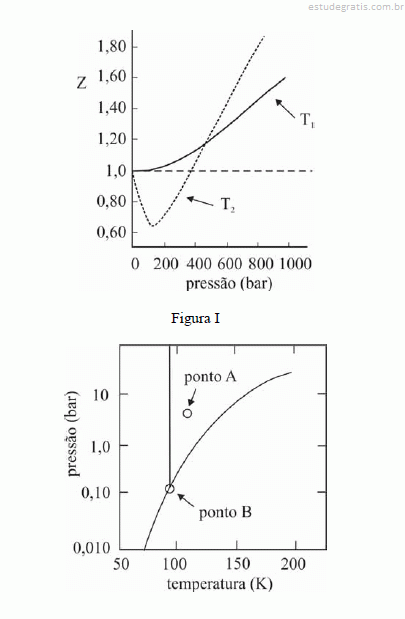
A figura I ilustra o gráfico do coeficiente de compressibilidade (Z) do CH4 (g) em função da pressão para duas temperaturas distintas (T1 e T2), e a figura II representa o diagrama de fases desse mesmo composto. A partir das figuras apresentadas, julgue os itens que se seguem.
Na temperatura T2, o CH4 (g), a 200 bar de pressão, ocupará um volume superior ao estimado pela equação dos gases ideais, o que demonstra que as forças atrativas predominam sobre as forças repulsivas.