Em um experimento colocou-se SO2Cl2(g) em um recipiente lacrado, mantido a 400 K. Nesta temperatura, a constante de equilíbrio Kp para a reação de decomposição deste gás: SO2Cl2(g) ↔ SO2(g) + Cl2(g) é 2,4 quando as pressões são medidas em atmosferas (atm). Determine a pressão parcial do gás cloro formado no equilíbrio a 400 K, se, neste experimento, a pressão do equilíbrio medida foi 3 atm.
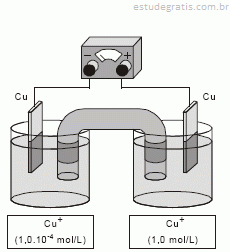
A diferença de potencial obtida na pilha, representada pela figura abaixo, no início de sua operação é
Os alcanos halogenados C3H7Br, C3H7Cl, C3H7I, CH3Cl, C2H5Cl, em ordem crescente de ponto de ebulição são:
Com base nas entalpias padrão (ΔH°) para as reações abaixo, determine a entalpia padrão para a reação de formação do etano a partir do carbono sólido e do gás hidrogênio.

É considerada(o) como parte dos investimentos fixos de uma indústria
O fato de que um equipamento perde o seu valor com o tempo devido à deterioração física ou aos avanços tecnológicos que fazem com que este equipamento se torne obsoleto é conhecido como
Os tratamentos de efluentes líquidos podem ser classificados como primários, secundários e terciários. Um exemplo de tratamento secundário é
Para medir a carga poluente de um efluente, são empregadas duas medidas: a demanda química de oxigênio (DQO) e a demanda bioquímica de oxigênio (DBO). Com relação a essas duas grandezas podese dizer: