A figura seguinte ilustra, em um diagrama de pressão vers...
A figura seguinte ilustra, em um diagrama de pressão versus volume, a expansão isotérmica reversível de um mol de um gás ideal, desde um estado inicial A, correspondente a uma pressão de 300 kPa e um volume de 8,00 L, até um estado final B, com pressão e volume iguais a 100 kPa e 20,00 L, respectivamente.
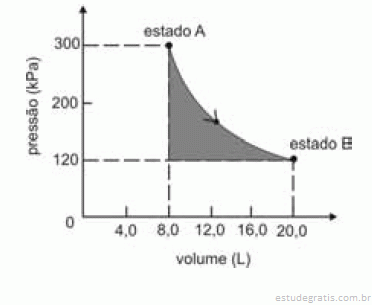
Com base nessas informações e considerando que a constante universal dos gases, R, seja igual a 8,3 .J.mol -1 K -1 e que os logaritmos naturais de 5 e 2 sejam iguais a 1,609 e 0,693, respectivamente, julgue os itens a seguir.
Considere que, após a referida transformação, o sistema tenha retornado ao estado A. Nessa situação, qualquer que seja o caminho de retorno, o calor trocado com as vizinhanças e o trabalho realizado pelo sistema durante o ciclo (estado A → estado B → estado A) são ambos iguais a zero, pois calor e trabalho são funções de estado termodinâmicas.
Comentários
Faça login para participar da discussão.
Cadastre-se Gratuitamente