Considere uma experiência hipotética em que uma barra de...
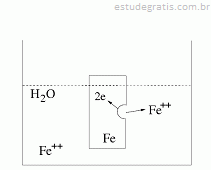
Considere uma experiência hipotética em que uma barra de ferro é colocada em água e ocorre somente a reação química anódica:
Fe → Fe ++ 2 e
em que "e" denota elétrons que se originam da reação química. Como os elétrons não podem ser conduzidos para longe do eletrodo é estabelecido um potencial elétrico "V" entre o interior do metal e a solução. Esse potencial pode ser medido relativamente a um eletrodo de referência padrão de hidrogênio com potencial Vo, para concentração unitária (1mol/litro) dos íons Fé++ em solução, por meio da lei logarítimica de Nernst
V = Vo + (a Log c ) / b
em que a é uma constante, b a valência do íon e c a concentração de íons Fé++ dada em moles de íon/litro.
Assinale a opção incorreta.
Comentários
Faça login para participar da discussão.
Cadastre-se Gratuitamente